Радикальная сополимеризация акрилат- и метакрилатгуанидинов с виниловыми мономерами
Рефераты по химии / Радикальная сополимеризация акрилат- и метакрилатгуанидинов с виниловыми мономерамиСтраница 7
Поэтому можно ожидать, что электростатическое притяжение протонированной (второй) аминогруппы ЭДА и метакрилатаниона должно дополнительно способствовать присоединению метакрилатаниона к активному центру, связанному водородной связью с неионизованной аминогруппой ЭДА. Существенный вклад в стабилизацию таких ассоциатов могут также вносить гидрофобные взаимодействия. Однако, при переходе к нейтральным рН (6,8-7,5) концентрация подобных ассоциатов, очевидно, уменьшается (вследствие ионизации самих карбоксильных групп в звеньях растущих цепей), что приводит к падению скорости полимеризации.
Схема 2
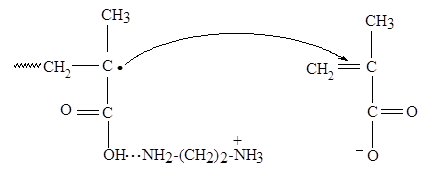
В щелочной области рН присутствие ЭДА и ИБА (рК = 10,4) приводит к более резкому, чем при добавлении NaOH, возрастанию скорости полимеризации метакрилатаниона с ростом рН. В рамках гипотезы о кинетической роли ионных пар это можно объяснить тем, что при рН > 7,5, когда макрорадикалы преимущественно ионизованы, происходит образование ионных пар на концах растущих цепей с участием карбоксилатанионов макрорадикалов и органических катионов, что способствует ускорению реакции роста цепи. В этих случаях, видимо, образованию ионных пар с участием этилендиаммония и изобутиламмония способствуют и гидрофобные взаимодействия, дополнительно стабилизирующие ионные пары.
По всей вероятности, гидрофобные эффекты ответственны также и за наблюдаемые значительные отличия в кинетике полимеризации акрилат- и метакрилатанионов в водных растворах, рН которых установлен добавлением триэтиламина. Существенно бóльший кинетический эффект с ростом рН при полимеризации метакрилатаниона авторы связали с установленными ранее доказательствами того, что для цепей ПМАК гидрофобные взаимодействия существенно выше, чем для ПАК [33] и предположили, что именно такие взаимодействия дополнительно стабилизируют ионные пары на концах ионизованных радикалов роста ПМАК.
Интересные результаты были получены в ходе кинетических исследований полимеризации рассматриваемых кислот при использовании в качестве нейтрализующего агента слабого неорганического основания NH4OH. Авторами было установлено, что, как при полимеризации АК, так и для МАК наблюдается более резкое увеличение скорости полимеризации. Особенно значительно это увеличение проявляется при полимеризации метакрилатаниона.
Обнаруженные различия в скоростях полимеризации МАК и АК в области рН = 6-9 в присутствии NaOH и NH4OH [10, 12] авторы объяснили специфичностью связывания ионов Na+ и NH4+ с ПМАК, что вытекает из рассмотрения кривых титрования соответствующих поликислот [19]. Существенно больший кинетический эффект (с ростом рН) при полимеризации метакрилатаниона также связали с ярко выраженными гидрофобными свойствами ПМАК (по сравнению с ПАК), предположив, что и в случае добавления NH4OH в реакционные растворы так же, как и в случае ЭДА и ИБА, гидрофобные взаимодействия должны дополнительно стабилизировать ионные пары на концах ионизованных радикалов ПМАК.
В работах этих же авторов [10,12] был обнаружен также качественно другой тип влияния нейтрализующего агента при полимеризации МАК в водных средах, когда рН реакционного раствора создавался добавлением в него слабого органического основания – пиридина (Py) (рКа – 5,19). Полимеризация метакриловой кислоты от рН в присутствии пиридинийионов заметно отличается от аналогичной зависимости, обнаруженной в растворе NaOH и других изученных нейтрализующих агентов – ЭДА, ИБА, NH4OH. Во всех указанных случаях наблюдали падение скорости полимеризации с ростом рН до 4,5.
Характерной особенностью обнаруженной зависимости является наличие острого максимума в интервале рН = 3,5-4,0, причем скорость реакции оказывается на порядок выше скорости полимеризации метакриловой кислоты в растворе NaOH при тех же значениях рН ([МАК] = 0,92 моль×л-1). Увеличение скорости происходит даже тогда, когда в растворах присутствует относительно небольшое количество пиридина. Для обеих концентраций максимальной скорости полимеризации соответствует исходное молярное отношение [Ру]/[МАК] = 0,23.
Информация о химии
Гиббс (Gibbs), Джозайя Уиллард
Американский физик и математик Джозайя Уиллард Гиббс родился в Нью-Хейвене, штат Коннектикут. Он окончил Йельский университет, где его успехи в греческом, латыни и математике были отмечены призами и премиями. В 1863 г. Гиббс получ ...
Классификация по атомному весу
Со времен Дальтона до 1860 в химии не было точного определения понятия атомного веса. Система, основанная на «эквивалентных весах», предложенная английским химиком Уильямом Волластоном (1766–1828), опиралась на с ...
Учёные изобрели самодвижущиеся наностержни
Изящное изобретение представляет собой самую крошечную химическую батарейку и электромотор в одном лице. Авторы работы полагают, что в будущем такие устройства смогут приводить в действие наномашины. Необычный мотор создаёт вдо ...


