Инструментальные методы анализа веществ
Рефераты по химии / Инструментальные методы анализа веществСтраница 5
Биамперометрическое титрование. Этот вид амперометрического титрования основан на использовании двух поляризуемых электродов – обычно платиновых, на которые подается небольшая разность потенциалов – 10–500 мВ. В этом случае прохождение тока возможно лишь при протекании обратимых электрохимических реакций на обоих электродах. Если хоть одна из реакций кинетически затруднена, происходит поляризация электрода, и ток становится незначительным.
Вольтамперные зависимости для ячейки с двумя поляризуемыми электродами приведены на рис. 3.2. В этом случае играет роль лишь разность потенциалов между двумя электродами. Значение потенциала каждого из электродов в отдельности остается неопределенным ввиду отсутствия электрода сравнения.
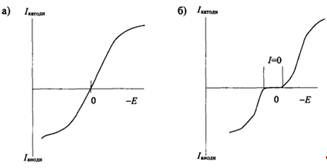
Рис 3.2 Вольтамперные зависимости для ячейки с двумя одинаковыми поляризуемыми электродами в случае обратимой реакции без перенапряжения (а) и необратимой реакции с перенапряжением (б).
В зависимости от степени обратимости электродных реакций можно получить кривые титрования различной формы.
а) Титрование компонента обратимой окислительно-восстановительной пары компонентом необратимой пары, например, иода тиосульфатом (рис. 3.3, а):
I2 + 2S2O32-![]() 2I- + S4O62-.
2I- + S4O62-.
До точки эквивалентности через ячейку протекает ток, обусловленный процессом:
2I- ![]() I2 + e-.
I2 + e-.
Ток возрастает вплоть до величины степени оттитрованности, равной 0,5, при которой оба компонента пары І2/І- находятся в одинаковых концентрациях. Затем ток начинает убывать вплоть до точки эквивалентности. После точки эквивалентности вследствие того, что пара S4O62-/S2O32- является необратимой, наступает поляризация электродов, и ток прекращается.
б) Титрование компонента необратимой пары компонентом обратимой пары, например, ионов As(III) бромом (рис. 3.3, б):
![]()
До точки эквивалентности электроды поляризованы, поскольку окислительно-восстановительная система As(V)/As(III) необратима. Через ячейку не протекает ток. После точки эквивалентности ток возрастает, поскольку в растворе появляется обратимая окислительно-восстановительная система Вr2/Вr-.
в) Определяемое вещество и титрант образуют обратимые окислительно-восстановительные пары: титрование ионов Fe(II) ионами Ce(IV) (рис. 3.3, в):
![]()
Здесь поляризации электродов не наблюдается ни на каком этапе титрования. До точки эквивалентности ход кривой такой же, как на рис. 3.3, а, после точки эквивалентности – как на рис. 3.3, б.
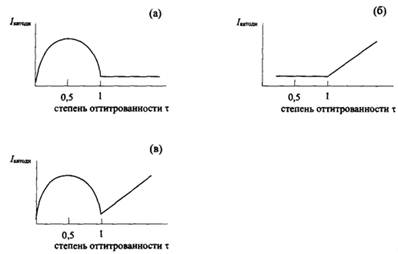
Рис. 3.3 Кривые биамперометрического титрования иода тиосульфатом (a), As(III) бромом (б) и ионов Fe(II) ионами Ce(IV) (в)
3.2 Задача: в электрохимическую ячейку с платиновым микроэлектродом и электродом сравнения поместили 10,00 смі раствора NaCl и оттитровали 0,0500 моль/дмі раствором AgNO3 объёмом 2,30 смі. Рассчитать содержание NaCl в растворе (%)
В растворе идет реакция:
Ag+ + Cl- =AgCl↓.
Тогда:
V(AgNO3) = 0,0023 (дм3);
n(AgNO3) = n(NaCl);
n(AgNO3)=c(AgNO3)•V(AgNO3)=0,0500•0,0023=0,000115,
или 1,15•104(моль).
n(NaCl) = 1,15•10-4 (моль);
Информация о химии
Сент-Клер Девиль (Sainte-Claire Deville), Анри Этьенн
Французский химик Анри Этьенн Сент-Клер Девиль родился в городе Сент-Томас на Виргинских островах. В 1843 г. окончил Парижский университет, получив степень доктора медицины; несколько лет занимался научными исследованиями в собств ...
Бэкон (Bacon), Роджер
Английский философ и естествоиспытатель Роджер Бэкон родился в Илчестере (графство Сомерсет). Получил образование в Оксфордском и Парижском университетах (магистр искусств, 1241). До 1247 г. преподавал в Парижском университете. Во ...
Sn — Олово
ОЛОВО (лат. Stannum), Sn, химический элемент с атомным номером 50, атомная масса 118,710. О происхождении слов «stannum» и «олово» существуют различные догадки. Латинское «stannum», которое иног ...


