Производство неконцентрированной азотной кислоты
Рефераты по химии / Производство неконцентрированной азотной кислотыСтраница 10
Средняя температура нитрозных газов [4]:
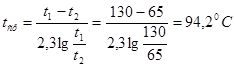
где t1-температура нитрозного газа на входе в аппарат, ![]()
t2- температура нитрозного газа на выходе из аппарата,![]()
Свободный объем [1, 4]:
![]()
![]()
где Dв- внутренний диаметр трубок, м;
L-длина трубного пространства, м;
n-количество трубок, шт;
Объемная скорость нитрозного газа:
Wс =![]() =45,77нм3/с;
=45,77нм3/с;
где 380000-мощность производства по проекту, т100%HNO3 /г; 330 рабочих дней в году; 24 часа в сутках.
Время пребывания газа в окислителе:[4]
![]()
Определяем степень окисления NO (α).Находим:
![]() ;
; ![]() ;
;
По справочным данным К при 94,2![]() [3]
[3]
Тогда ![]()
где К-константа скорости реакции, а-начальная концентрация NO, мольн. доли, ![]() -общее давление, атм.
-общее давление, атм.
По номограмме В.А. Каржавина [3] определяем практическую степень окисления оксида азота: x=0,47.
Степень приближения практической степени превращения к равновесной:
![]() 99,81%
99,81%
x 47% x=![]() x=47%
x=47%
Определяем практический состав газа.
Окисляется монооксида азота:
![]() ;
;
Остается:
![]() ;
;
Расходуется кислорода:
![]() ;
;
Остается кислорода:
![]() ;
;
Содержание NO2 в нитрозном газе на выходе из аппарата:
241,01+55,01=296,02.
Таблица 3.2
Материальный баланс процесса окисления NO в NO2 в холодильнике-конденсаторе
|
Приход |
Расход | ||||||||
|
Компонентный состав |
нм3/т |
% |
кг/т |
% |
Компонентный состав |
нм3/т |
% |
кг/т |
% |
|
NO |
117,05 |
3,09 |
223,62 |
5,61 |
NO |
62,04 |
1,65 |
248,35 |
6,23 |
|
NO2 |
241,01 |
6,36 |
148,55 |
3,73 |
NO2 |
296,02 |
7,88 |
161,23 |
4,05 |
|
O2 |
135,19 |
3,57 |
186,37 |
4,68 |
O2 |
104,17 |
2,77 |
148,96 |
3,74 |
|
N2 |
2691,38 |
71,03 |
3364,23 |
84,44 |
N2 |
2691,38 |
71,61 |
3364,23 |
84,44 |
|
H2O |
604,54 |
15,95 |
61,44 |
1,54 |
H2O |
604,54 |
16,09 |
61,44 |
1,54 |
|
Всего: |
3789,17 |
100,00 |
3984,21 |
100,00 |
Всего: |
3758,15 |
100,00 |
3984,21 |
100,00 |
Информация о химии
C — Углерод
УГЛЕРОД (лат. Carboneum), С, химический. элемент IV группы периодической системы Менделеева, атомный номер 6, атомная масса 12,011. Свойства: при обычных условиях углерод химически инертен; при высоких температурах соединяется с ...
Dy — Диспрозий
ДИСПРОЗИЙ (лат. Dysprosium), Dy, химический элемент III группы периодической системы, атомный номер 66, атомная масса 162,50, относится к лантаноидам. Свойства: металл. Плотность 8,66 г/см3; tпл 1409 °C. Компонент специальных ...
Кекуле фон Штрадонитц (Kekule von Stradonitz), Фридрих Август
Немецкий химик Фридрих Август Кекуле фон Штрадониц родился в Дармштадте в семье чиновника. В юности Кекуле собирался стать архитектором. Он начал изучать архитектуру в Гисенском университете, но, прослушав курс лекций Ю.Либиха в д ...


