Исследование фазовых эффектов в бинарных азеотропных смесях
Рефераты по химии / Исследование фазовых эффектов в бинарных азеотропных смесяхСтраница 10
U= TS-PV+ μ1x1+ μ2x2 2.11
После дифференцирования получаем
dU= TdS + SdT – PdV – VdP + μ1 dx1 + x1dμ1 + μ2 dx2 + x2dμ2 2.12
Но так как
dU= TdS - PdV+ μ1 dx1 + μ2 dx2 2.13
то очевидно
SdT-VdP+ x1dμ1+ x2dμ2 =0 2.14 Если применять почленно преобразование Лежандра, то, учитывая, что при этом меняется в каждом случае знак, получим
-SdT+VdP- x1dμ1- x2dμ2 =0 2.15
Автор [14] не видит разницы между уравнениями в форме 2.14 и 2.15, поэтому приводит уравнение 2.15, очевидно считая, что если правая часть равна нулю, то обе формы идентичны.
Как уже говорилось, нулевой потенциал есть скалярное произведение вектора
< S, V, x1, x2 >
на вектор < dT, dP, dμ1, dμ2 >
Учитывая, что это скалярное произведение равно нулю, векторы-сомножители ортогональны друг другу.
Так как, вектор < dT, dP, dμ1, dμ2 > есть вектор параметров, которые могут изменяться независимо, очевидно вектор < S, V, x1, x2 > может быть представлен двояко < S, -V, x1, x2 > или <- S, V, -x1, - x2 >
![]() Оба представления получаются равнозначными, так как эти векторы ортогональны. Проиллюстрируем это при условии Р=соnst. В этом случае имеем
Оба представления получаются равнозначными, так как эти векторы ортогональны. Проиллюстрируем это при условии Р=соnst. В этом случае имеем
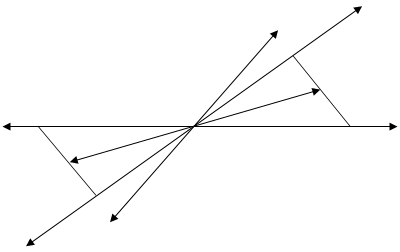 < S, x1, x2 > и <- S, -x1, - x2 > S
< S, x1, x2 > и <- S, -x1, - x2 > S
S х1 х2 х1
х
-х2 х2
-х
-S -х1 -х2
-х1
- S
Рис.2.10. Взаимное расположение вектора состава
То есть, в случае перемены знаков произведение знака не меняет, если давление постоянно.
Выведем уравнение Ван-дер-Ваальса для жидкой фазы. Исходим из того, что в этом случае начальная точка вектора конноды при Р=соnst будет точка, соответствующая свойствам жидкой фазы. В связи с этим правилом запишем уравнения 2.14 для паровой и жидкой фаз при Р=соnst:
Sп dT + у1 dμ1 + у2 dμ2=0 2.16
Sж dT + x1 dμ1 + x2 dμ2=0 2.17
Отнимем от первого уравнение второе и получим:
(Sп- Sж) dT + (у1- х1)dμ1 +(у2- x2)dμ2=0 2.18
Таким образом, мы, получим произведение конноды жидкость-пар < Sп- Sж, у1- х1, у2- x2> на вектор параметров < dT, dμ1, dμ2 >, которые в условиях термодинамического равновесия одинаковы, как в жидкой, так и в паровой фазах.
Так как х1+х2=1 и у1+у2=1, то очевидно
у1- х1+ у2- x2=0
т.е. у2- x2= -(у1- х1) 2.19
Следовательно, с учетом 2.19
(Sп- Sж) dT + (у1- х1) (dμ1-dμ2)=0 2.20
В уравнении 2.20 dT и d(μ1-μ2) полные дифференциалы.
Для перехода к координатам функции g необходимо выразить d(μ1-μ2), как функции х1 и Т (Р=соnst)
d(μ1-μ2) =![]()
![]() 2.21
2.21
Подставляя в уравнение 2.20 значение d(μ1-μ2) из 2.21, получим
![]() 2.22
2.22
![]() можно представить в виде
можно представить в виде ![]() . В самом деле,
. В самом деле, ![]() ,
, ![]() . Но
. Но ![]() согласно соотношению Максвелла (смешанные производные не зависят от порядка дифференцирования).
согласно соотношению Максвелла (смешанные производные не зависят от порядка дифференцирования).
Информация о химии
Нейрохимия
Нейрохимия — раздел биохимии, изучающий химические и клеточные механизмы деятельности нервной системы. Различают общую нейрохимию — изучающую химические процессы нервной системы вне связи с конкретным механизмы деятел ...
Пастер (Pasteur), Луи
Французский микробиолог и химик Луи Пастер родился в Доле (Юра, Франция). В 1847 г. он окончил Высшую нормальную школу в Париже, в 1848 г. защитил докторскую диссертацию. Преподавал естественные науки в Дижоне (1847–1848), б ...
Химический элемент хром
Элемент №24. Один из самых твердых металлов. Обладает высокой химической стойкостью. Один из важнейших металлов, используемых в производстве легированных сталей. Большинство соединений хрома имеет яркую окраску, причем ...


