Получение изопропанола
Рефераты по химии / Получение изопропанолаСтраница 8
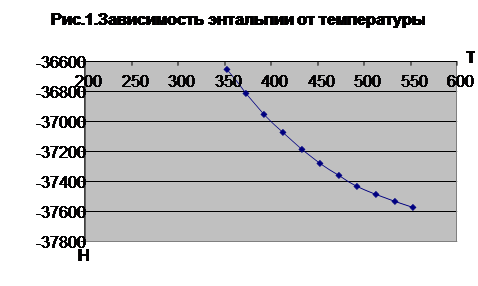

Вывод:
Таким образом в ходе проведенных термодинамических расчетов установили, что данная химическая реакция в данном интервале температур (от 353 до 553 К) имеет H<0, следовательно реакция является экзоотермической.
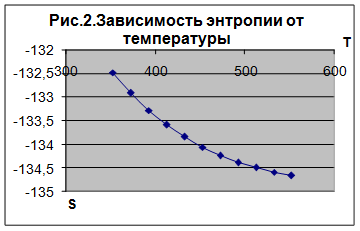
В ходе химической реакции происходит уменьшение энтропии (S<0), следовательно тепловое (хаотичное) движение молекул уменьшается
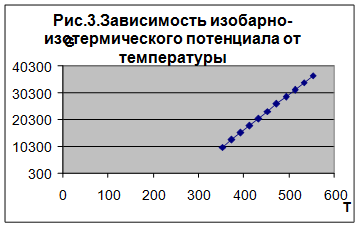
Изменение изобарно-изотермического потенциала от 353 К до 553 К положительное, следовательно при заданном интервале реакция протекает самопроизвольно. С ростом температуры G увеличиваетсяся, значит реакцию следует проводить при пониженных температурах.
5
. Расчет
константы равновесия и равновесного состава реагирующих веществ
Все обратимые химические реакции во времени стремятся к равновесию, при котором скорости прямого и обратного процессов уравновешиваются, в результате чего соотношение компонентов в реакционной массе остается неизменным, пока в системе не изменяются параметры технологического режима (температура, давление, концентрации компонентов). При изменении параметров технологического режима равновесие в системе нарушается и самопроизвольно переходит в новое состояние, которое характеризуется новым соотношением компонентов реакционной массы.
Зная значения константы равновесия, можно легко рассчитать состав реакционной массы обратимых химических реакции и определить максимально возможный (теоретический) выход целевого продукта или равновесную степень превращения.
Равновесный состав реакционной смеси простых обратимых реакции находят путем решения уравнении закона действующих масс.
Для основной реакции и заданных давлении и температуры определить константу равновесия Kp. Рассчитать равновесный состав реакционной массы. При расчете использовать данные материального баланса.
A B C
Дано: : CH2=CH-CH3+H2O =CH3-CH(OH)-CH3
Pобщ=1,7 Мпа
T=185o C = 458К
1. Рассчитываем значение константы равновесия для данной реакции при данной температуре:
∆H463=-36130-29,34 (463-298)+78,41∙10-3 (4632-2982) /2-50,84∙10-6∙
(4633-2983) /3-0,33∙105(1/298-1/463)=-37321,3 Дж/моль
∆S463=-130.86-29.34 ln(463/298)+78.41∙10-3(463-298)-50.84∙10-6 ∙
∙(4632-2982)/2-0.33∙105 (1/2982-1/4632) /2=-134.151 Дж/моль∙к
ΔG463=-37321,3+463∙134.151=24790,613 Дж/моль
Kp473=exp(-24790,613/8,314ּ463)=0.0016
2. Запишем выражение для константы равновесия для заданной реакции:
Kp = PC
PB PA
Kp= KNּPобщ∆ν
Kp = NC ּP-1
NB NA
3. Составим баланс молей состояния равновесия:
Таблица Баланс молей
|
nA |
nB |
nC | |
|
исх. смесь |
17.92 |
0.53 |
- |
|
образовалось |
- |
- |
X |
|
израсходовалось |
X |
X |
- |
|
сост. равновесия |
17.92-X |
0.53-X |
X |
∑ni=17.92-X+0.53-X+X=18.45-X
NA= 17.92-X
18.45-X
NB= 0.53- X
18.45-X
NC= X
18.45-X
4.Подставим значения мольных долей в уравнение для константы равновесия:
![]()
―――――――――――=0.0016
![]() *P
*P
2721X2-50202.45X+25840=0
1.36X2-25.1X+12.92=0
Решая квадратное уравнение получаем два корня :
X1=17.926
X2=0.5294
Выбираем корень X2=0.5294
nA=14,1-5,722ּ10-4=14,099428 моль
nB=5,722ּ10-4
nC=22,888ּ10-4
NA=![]()
NB=![]()
Информация о химии
Mg — Магний
МАГНИЙ (лат. Magnesium), Mg (читается «магний»), химический элемент IIА группы третьего периода периодической системы Менделеева, атомный номер 12, атомная масса 24,305. Природный магний состоит из трех стабильных нукл ...
Химия полимеров
Химия полимеров — раздел химии, в котором изучаются химические свойства полимеров. Делится на разделы: физическая химия полимеров, структурная и т. д. Синоним — химия высокомолекулярных соединений — раздел орган ...
Cm — Кюрий
КЮРИЙ (лат. Curium), Cm, химический элемент III группы периодической системы, атомный номер 96, относится к актиноидам. Свойства: серебристый металл, плотность 13,51 г/см3, tпл 1358 °С. Радиоактивен, наиболее устойчивый изото ...


