Производство неконцентрированной азотной кислоты
Рефераты по химии / Производство неконцентрированной азотной кислотыСтраница 8
Расчет ведем на 1000 кг 100,00%-й HNO3, получаемой в технологическом процессе.
Температура нитрозных газов на входе в холодильник, 0С 130.
Температура нитрозных газов на выходе из холодильника, 0С 65.
Температура охлаждающей воды , 0С 40.
Давление в холодильнике, МПа 0,36
Диаметр холодильника-конденсатора, м 2,2.
Поверхность теплообмена, м2 1428.
Наружный диаметр трубок, м 0,05.
Расход газа, поступающего в холодильник-конденсатор 3789,17нм3/т [1].
Зная состав газа, можно определить расход каждого компонента:
|
Компонентный состав |
кг/т |
нм3/т |
об.% |
|
NO |
223,62 |
117,05 |
3,09 |
|
NO2 |
148,55 |
241,01 |
6,36 |
|
O2 |
186,37 |
135,19 |
3,57 |
|
N2 |
3364,23 |
2691,38 |
71,03 |
|
H2O |
61,44 |
604,54 |
15,95 |
|
Всего: |
3984,21 |
3789,17 |
100 |
Расчет материального баланса процесса окисления нитрозного газа
Равновесие и скорость окисления оксида азота II.
NO+1/2O2=NO2 ΔrH(298) =112кДж/моль (3.1)
Зависимость константы равновесия от температуры по данным М. Боденштейна [3] выражается следующим уравнением:
LgK =Lg![]() +1,75LgT-0,0005T+2,839 (3.2)
+1,75LgT-0,0005T+2,839 (3.2)
Для расчета равновесной степени окисления оксида азота (II) выразим парциальные давления газов, входящие в уравнение равновесия, через общее давление в зависимости от начальной концентрации газа[3]:
Введем обозначения:
2a- начальная концентрация NO, мольн.доли;
b- начальная концентрация O2, мольн.доли;
xр- равновесная степень окисления NO, доли единицы;
Робщ- общее давление газа, атм.
Равновесные концентрации компонентов газовой смеси согласно реакции (3.1)составят:
|
Компонент |
Вход |
Выход |
|
NO |
2a |
2а(1-xp) |
|
O2 |
b |
b-axp |
|
NO2 |
- |
2axp |
|
Всего: |
1 |
1-axp |
Тогда парциальные давления компонентов газа при общем давлении 3,6 атм. в момент равновесия будут равны:
PNO=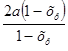 Pобщ;
Pобщ;
РO2=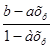 Pобщ;
Pобщ;
РNO2=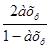 Pобщ;
Pобщ;
Подставляя значения парциальных давлений в уравнение равновесия, получим:
![]() =
=![]() P (3.3)
P (3.3)
Определим равновесную степень окисления оксида азота (II) для газа, содержащего 3,09% NO и 3,57% (об) O2 при 3,6 атм.
Информация о химии
Sn — Олово
ОЛОВО (лат. Stannum), Sn, химический элемент с атомным номером 50, атомная масса 118,710. О происхождении слов «stannum» и «олово» существуют различные догадки. Латинское «stannum», которое иног ...
Ядерная химия
Ядерная химия — часть химии высоких энергий, раздел физической химии — изучает ядерные реакции и сопутствующие им физико-химические процессы, устанавливает взаимосвязь между физико-химическими и ядерными свойствами вещ ...
Гитон де Морво (Guyton de Morveau), Луи Бернар
Французский химик и политический деятель Луи Бернар Гитон де Морво родился в городе Дижоне, Бургундия. Получил блестящее юридическое образование; уже в восемнадцатилетнем возрасте занял место генерального адвоката при дижонском па ...


