Синтез наноразмерного ТiO2 из алкоксидов титана, исследование дисперсности и фазового состава
Рефераты по химии / Золь-гель метод / Синтез наноразмерного ТiO2 из алкоксидов титана,
исследование дисперсности и фазового составаСтраница 1
Для синтеза ТiO2 из алкоксидов титана наиболее предпочтительны тетраизопропоксид (далее изопропоксид) титана и тетрабутоксид (далее бутоксид) титана.
Коллоидные растворы ТiO2, различающиеся размером частиц и устойчивостью, были получены из Ti(OPri)4, модифицированного ацетилацетоном, при использовании органических растворителей различной полярности и с разным молярным объемом. По данным рентгенофазового анализа (РФА), независимо от природы используемого при гидролизе органического растворителя все свежеприготовленные золи, полученные с добавлением или без добавления ацетилацетона, содержат аморфный ТiO2, который превращается в нанокристаллическую фазу анатаза при нагревании до 450°С. Однако использование растворителей с малым молярным объемом и модифицирование предшественника ацетилацетоном приводят к стабилизации коллоидного раствора ТiO2, что и является основным результатом цитируемой работы. Методом ИК-спектроскопии показано образование хелатного комплекса между изопропоксидом титана и ацетилацетоном (рис. 6), что, по мнению авторов, приводит к замедлению гидролиза и конденсации и, следовательно, к уменьшению степени агломерации частиц ТiO2, а влияние растворителя на размер агрегатов (рис. 7) объяснено с точки зрения параметров растворимости Хансена. Установлены параметры растворимости Хансена для ТiO2, полученного в различных растворителях в присутствии ацетилацетона, которые могут быть полезны при синтезе стабильного коллоидного ТiO2.
Данные о размере частиц ТiO2 в коллоидных растворах и степени их агрегации в сухих порошках получены с помощью методов светового рассеяния, сканирующей электронной микроскопии (СЭМ) и ПЭМ.
Изопропоксид титана, диэтаноламин (ДЭА) и этанол (в соотношении 3:1:20 по объему) были использованы в качестве исходных реагентов для получения золя ТiO2 При этом важен порядок смешения компонентов, так как введение EtOH перед добавлением ДЭА приводит к очень быстрому осаждению ТiO2, что обусловлено высокой реакционной способностью алкоксида в этаноле. Поэтому сначала смешивают половину объема спирта с ДЭА, затем добавляют изопропоксид титана, перемешивают в течение 30 мин и только после этого добавляют остальное количество ЕtOН, полученную смесь интенсивно перемешивают при комнатной температуре. Золь стабилен в течение недели, после чего переходит в гель. Отмечено, что при уменьшении времени перемешивания золя наблюдается значительное увеличение его стабильности. Стабильность золя также существенно возрастает в условиях низкой влажности. В ходе высушивания образуется ксерогель, который существенно «усаживается» по сравнению с исходным гелем (происходит уменьшение объема в 5- 10 раз).
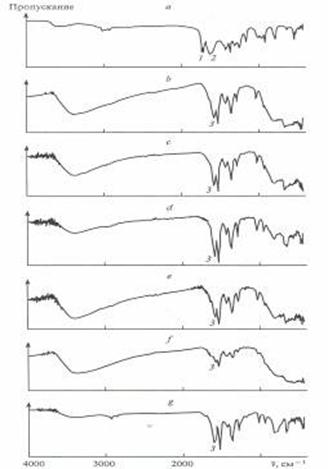
Рис. 6. ИК-Спектры ацетилацетона (а) и золей диоксида титана, полученных в присутствии ацетилацетона в различных органических растворителях: в ТГФ (b), ацетоне (с), бутаноле (d), хлороформе (e), толуоле (f), гексане (g). 1 — пик группы С=0 кето-формы, 2 — пик группы С = 0 енольной формы, 3 — пик группы С=0 хелатного комплекса.
Фаза чистого анатаза с размером частиц 10-20 нм может быть получена в результате очень простого низкотемпературного (100°С) синтеза в автоклаве с использованием лишь воды в качестве среды и изопропоксида титана как предшественника (без добавок). Размер, форма и фазовый состав частиц изучены методами РФА и ПЭМ.
В работе исследованы наночастицы ТiO2, полученные гидролизом Ti(OPri)4 при различных значениях рН среды. Для дальнейшего приготовления нанопорошка с узким распределением частиц по размерам была применена пептизация конечной суспензии. Отмечено влияние рН на размер и морфологию частиц нанопорошков. По данным РФА, СЭМи ПЭМ, свежеприготовленные порошки полностью состояли из кристаллической фазы анатаза. Лишь порошок, полученный из сильнокислого раствора, состоял из мелких аморфных сферических частиц.[3,945] Показано, что переход анатаза в рутил происходит при температурах ниже 600°С.
В исследовании для приготовления коллоидного раствора TiO2 использованы изопропоксид титана и смесь изопропилового спирта с соляной кислотой. В результате гидролиза изопропоксида получался коллоидный раствор ТЮ2 с концентрацией 0.9 моль *л -1.
Авторы работы для получения наноструктурных пленок готовили золь TiO2 из изопропоксида титана и смеси этанола с соляной кислотой (молярное соотношение Тi(OPri)4: НС1: EtOH : Н20 = 1:1.1:10 :10) с последующим добавлением раствора метилцеллюлозы (МЦ). Показано, что при увеличении содержания воды и разбавлении золя гелеобразование замедляется.
Из золей диоксида титана прокаливанием получали нано-порошок TiO2, из которого готовили гомогенные суспензии, необходимые для создания пленок. Стабильность суспензий TiO2 была исследована по скорости седиментации. Варьировалась концентрация нанопорошка анатаза в жидкой среде (5-10 мас.%) с добавлением и без добавления МЦ. Показано, что скорость оседания нанопорошка ТiO2 резко уменьшается в присутствии МЦ. Так, в 5- и 10%-ной суспензиях без добавления МЦ оседание происходит в течение 1 ч и 30 мин соответственно, в присутствии МЦ 5%-ная суспензия устойчива в течение 3 сут, а 10%-ная — в течение 10 ч. Таким образом, МЦ выступает в качестве диспергирующего агента. Данные СЭМ свидетельствуют о заметном улучшении гомогенности и однородности пленок ТiO2 и увеличении их удельной поверхности в присутствии МЦ .
Информация о химии
Геохимия
Геохимия — наука о химическом составе Земли и планет (космохимия), законах распределения и движения элементов и изотопов в различных геологических средах, процессах формирования горных пород, почв и природных вод. Важнейшие ...
Gd — Гадолиний
ГАДОЛИНИЙ (лат. Gadolinium), Gd, химический элемент III группы периодической системы, атомный номер 64, атомная масса 157,25, относится к лантаноидам. Свойства: металл, плотность 7,895 г/см3, tкип 1312 °С. Ферромагнетик (ниже ...
Хроматография
Хроматографический метод – физико-химический метод разделения компонентов сложных смесей газов, паров, жидкостей или растворенных веществ, основанный на использовании сорбционных процессов в динамических условиях. К ...


