Инструментальные методы анализа веществ
Рефераты по химии / Инструментальные методы анализа веществСтраница 8
– при анализе: SВ=9,38 смІ, VВ=47 ммі, qСТ=0,00465 г, SСТ=4,51 смІ
SСТ/SВ = k•(qСТ/ qВ);
k = (SСТ/SВ)/(qСТ/ qВ) = (8,47/6,38)/(0,00869/0,00735) = 1,123;
qВ = k•qСТ•(SВ/SСТ) = 1,123•0,00465•(9,38/4,51) = 0,01086 г.
x, % = k•r•(SВ/SСТ)•100;
r = qСТ/ qВ = 0,00465/0,01086 = 0,4282;
x, % = 1,123•0,4282•(9,38/4,51) = 100%.
5.
Фотометрическое титрование
5.1
Фотометрическое титрование. Сущность и условия титрования. Кривые титрования. Преимущества фотометрического титрования в сравнении с прямой фотометрией
Фотометрические и спектрофотометрические измерения можно использовать для фиксирования конечной точки титрования. Конечная точка прямого фотометрического титрования появляется в результате изменения концентрации реагента и продукта реакции или обоих одновременно; очевидно, по меньшей мере, одно из этих веществ должно поглощать свет при выбранной длине волны. Косвенный метод основан на зависимости оптической плотности индикатора от объема титранта.
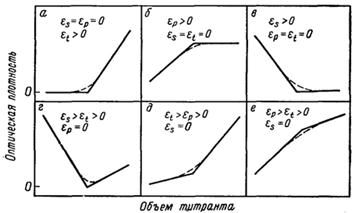
Рис. 5.1 Типичные кривые фотометрического титрования. Молярные коэффициенты поглощения определяемого вещества, продукта реакции и титранта обозначены символами еs, еp, еt соответственно
Кривые титрования. Кривая фотометрического титрования представляет собой график зависимости исправленной оптической плотности от объема титранта. Если условия выбраны правильно, кривая состоит из двух прямолинейных участков с разным наклоном: один из них соответствует началу титрования, другой – продолжению за точкой эквивалентности. Вблизи точки эквивалентности часто наблюдается заметный перегиб; конечной точкой считают точку пересечения прямолинейных отрезков после экстраполяции.
На рис. 5.1 приведены некоторые типичные кривые титрования. При титровании непоглощающих веществ окрашенным титрантом с образованием бесцветных продуктов в начале титрования получается горизонтальная линия; за точкой эквивалентности оптическая плотность быстро растет (рис. 5.1, кривая а). При образовании окрашенных продуктов из бесцветных реагентов, наоборот, сначала наблюдается линейный рост оптической плотности, а затем появляется область, в которой поглощение не зависит от объема титранта (рис. 5.1, кривая б). В зависимости от спектральных характеристик реагентов и продуктов реакции возможны также кривые других форм (рис. 5.1).
Чтобы конечная точка фотометрического титрования была достаточно отчетливой, поглощающая система или системы должны подчиняться закону Бера; в противном случае нарушается линейность отрезков кривой титрования, необходимая для экстраполяции. Необходимо, далее, ввести поправку на изменение объема путем умножения оптической плотности на множитель (V+v)/V, где V – исходный объем раствора, a v – объем добавленного титранта.
Фотометрическое титрование часто обеспечивает более точные результаты, чем прямой фотометрический анализ, так как для определения конечной точки объединяются данные нескольких измерений. Кроме того, при фотометрическом титровании присутствием других поглощающих веществ можно пренебречь, поскольку измеряется только изменение оптической плотности.
5.2 Задача: навеску дихромата калия массой 0,0284 г растворили в мерной колбе вместимостью 100,00 смі. Оптическая плотность полученного раствора при лmax=430 нм равна 0,728 при толщине поглощённого слоя 1 см. вычислить молярную и процентную концентрацию, молярный и удельный коэффициенты поглощения этого раствора
Информация о химии
Агрикола (Agricola), Георг
24 марта 1490 г. – 21 ноября 1555 г. Георг АгриколаНемецкий учёный в области горного дела и металлургии Георг Агрикола [настоящая фамилия Бауэр (Bauer); лат. agricola – земледелец, перевод немецкого слова Bauer] родил ...
Жолио-Кюри (Joliot-Curie), Ирен
Французский физик Ирен Жолио-Кюри родилась в Париже. Она была старшей из двух дочерей Пьера Кюри и Марии Склодовской-Кюри. Мари Кюри впервые получила радий, когда Ирен был всего год. Приблизительно в это же время дед Ирен по линии ...
Гальвани (Galvani), Луиджи
Итальянский анатом и физиолог Луиджи Гальвани, один из основателей учения об электричестве, основоположник электрофизиологии, родился в Болонье. В 1759 г. окончил Болонский университет, в котором изучал сначала богословие, а затем ...


