Инструментальные методы анализа веществ
Рефераты по химии / Инструментальные методы анализа веществСтраница 2
Люминесцентный или флуоресцентный анализ – основан на флуоресценции веществ, которые подвергаются облучению ультрафиолетовым светом. При этом измеряется интенсивность излучаемого или видимого света.
Пламенная фотометрия (фотометрия пламени) – основана на распылении раствора исследуемых веществ в пламени, выделении характерного для анализируемого элемента излучения и измерении его интенсивности. Метод используют для анализа щелочных, щелочноземельных и некоторых других элементов.
Хроматографические методы
анализа основаны на использовании явлений избирательной адсорбции. Метод применяют в анализе неорганических и органических веществ для разделения, концентрирования, выделения отдельных компонентов из смеси, очистки от примесей.
Радиометрические методы
анализа основаны на измерении радиоактивного излучения данного элемента.
Масс-спектрометрические
методы анализа основаны на определении масс отдельных ионизированных атомов, молекул и радикалов, в результате комбинированного действия электрического и магнитного полей. Регистрацию разделенных частиц проводят электрическим (масс-спектрометрия) или фотографическим (масс-спектрография) способами. Определение проводят на приборах – масс-спектрометрах или масс-спектрографах.
Примеры инструментальных методов анализа для качественного анализа веществ: рентгено-флуоресцентный, хроматография, кулонометрия, эмиссионный, пламенная фотометрия и т.д.
2. Потенциометрическое титрование
2.1 Сущность потенциометрического титрования. Требования к реакциям. Примеры реакций окисления-восстановления, осаждения, комплексообразования и соответствующие им электродные системы. Графические способы определения конечной точки титрования
Потенциометрическое титрование основано на определении эквивалентной точки по изменению потенциала на электродах, опущенных в титруемый раствор. При потенциометрическом титровании используют электроды как неполяризующиеся (без протекания через них тока), так и поляризующиеся (с протеканием через них тока).
В первом случае в процессе титрования определяется концентрация в растворе одного из ионов, для регистрации которого имеется подходящий электрод.
Потенциал Ех на этом индикаторном электроде устанавливается согласно уравнению Нернста. Например, для реакций окисления – восстановления уравнение Нернста выглядит следующим образом:
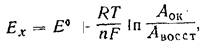
где Ех – потенциал электрода в данных конкретных условиях; Aок– концентрация окисленной формы металла; Aвосст – концентрация восстановленной формы металла; Е0 – нормальный потенциал; R – универсальная газовая постоянная (8,314 дж/(град•моль)); Т – абсолютная температура; n – разность валентностей окисленной и восстановленной форм ионов металла.
Для образования электрической цепи в титруемый раствор помещают второй так называемый электрод сравнения, например каломельный, потенциал которого в процессе реакции остается постоянным. Потенциометрическое титрование на неполяризующихся электродах помимо упомянутых реакций окисления – восстановления используется также при реакциях нейтрализации. В качестве индикаторных электродов при реакциях окисления-восстановления применяют металлы (Pt, Wo, Mo). При реакциях нейтрализации применяют чаще всего стеклянный электрод, имеющий в широкой области характеристику, аналогичную водородному электроду. Для водородного электрода зависимость потенциала от концентрации ионов водорода выражается следующей зависимостью:
Информация о химии
Ta — Тантал
ТАНТАЛ (лат. Tantalum), Та, химический элемент V группы периодической системы, атомный номер 73, атомная масса 180,9479. Свойства: светло-серый с синеватым отливом металл, тяжелый и тугоплавкий; плотность 16,6 г/см3, tпл 3014 &de ...
Натта (Natta), Джулио
Итальянский химик Джулио Натта родился в семье известного адвоката и судьи Франсиско Натта и Елены (Чреспи) Натта в Империи, курортном городке на побережье Средиземного моря. Мальчик рос в близлежащем городе Генуе. Натта было 12 л ...
Юри (Urey), Гарольд Клейтон
Американский химик Гарольд Клейтон Юри родился в Уолкертоне (штат Индиана), в семье Коры Ребекки (Рейноул) и Сэмуэла Клейтона Юри. Его отец, священник и школьный учитель, умер, когда мальчику было шесть лет, и мать Юри вышла замуж ...


