Исследование твердых электролитов
Рефераты по химии / Исследование твердых электролитовСтраница 20
 В
В
 Г
Г
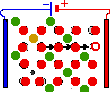
Цветом обозначены:
Зелёный — анион M, Красный — ион G, Жёлтый — анион M *, Фиолетовый — ион M*, Красный с белой точкой — вакансия
Двумерная решётка соединения типа MG2 (например, ZrО2) (А). Ионы элементов G и M образуют регулярные структуры — кристаллические подрешётки. Если смешать два соединения MG2 и M*G (скажем, СаО), в анионной подрешётке G появятся пустые места — вакансии (Б). Соседние катионы при достаточной энергии станут занимать пустые места, и вакансии начнут хаотично двигаться (направление указано стрелками) по кристаллу (В). Если к кристаллу приложить постоянное напряжение, вакансии устремятся к положительному электроду — аноду (Г). Через кристалл — твёрдый электролит — пойдёт электрический ток, обусловленный движением зарядов только одного знака.
Твёрдые электролиты всегда находятся в атмосфере определённых газов, состав которой меняет их свойства. Чтобы понять, в чём тут дело, вспомним, что такое динамическое равновесие. В жидкости, например, всегда есть "быстрые" молекулы, которые с её поверхности переходят в пар. Но и из пара молекулы возвращаются в жидкость — между ними происходит непрерывный обмен молекулами. Пар находится в равновесии с жидкостью, и, чтобы подчеркнуть, что оно сопряжено с движением на молекулярном уровне, его называют динамическим.
Характер обмена между твёрдым телом и газом сложнее. Ион кислорода в поверхностном слое превращается в нейтральный атом. Два атома соединяются в молекулу кислорода, которая отрывается от поверхности и переходит в газ. Возвращение кислорода из газа в твёрдое тело происходит в обратном порядке. Обе эти реакции идут одновременно: между электролитом и газом, содержащим определённое количество кислорода, существует динамическое равновесие. Оно нарушается, когда концентрация кислорода в газе меняется. Итак, твёрдый электролит в виде смеси оксидов циркония и кальция проводит ток только при высоких температурах. Поэтому лампы Нернста включали, предварительно сильно прогрев их стержень. И появление в 1905 году лампы "немедленного действия" с вольфрамовой нитью предопределило её абсолютный успех. Однако известно, что кое-где и сегодня можно встретить странный электрический фонарь, который нужно поджигать спичкой. Это, судя по всему, лампы Нернста, дожившие до наших дней: твёрдые растворы на основе диоксида циркония — исключительно стойкие вещества, они могут работать на воздухе десятилетиями, не окисляясь. Кстати, вполне современные печи с такими нагревателями были разработаны в свердловском Восточном институте огнеупоров в начале 80-х годов.
Главное предназначение твёрдых оксидных электролитов виделось в создании топливных элементов — химических источников тока, в которых энергия газа непосредственно превращается в электрическую. Топливные элементы — близкие родственники гальванических элементов. Но те служат, пока в их электролите и электродах есть активные вещества, а топливные элементы могут работать сколь угодно долго, пока к ним подводится горючее. Систематические исследования твёрдых оксидных электролитов начались в Германии в начале 50-х годов, а с конца 50-х развернулись в СССР, США и Канаде. В нашей стране эти работы с самого начала вёл Институт химии Уральского филиала АН СССР (Свердловск, ныне Екатеринбург), и школа высокотемпературной электрохимии твёрдых электролитов, созданная на Урале, стала уникальной по широте охвата проблемы и глубине её изучения.
Устройства с твёрдыми оксидными электролитами

Цветом обозначены:
Пробирка из ТОЭ, Корпус, Электроды, Нагреватель, Теплоизоляция, Стрелки — потоки газа
Схема электрохимического устройства. Пробирка из твёрдого оксидного электролита с металлическими электродами на стенке помещена в замкнутый объём, окружённый теплоизоляцией. Рабочую температуру около 1000°С создает нагреватель. Внутрь пробирки и в окружающий её объём подаётся газ. Это несложное устройство может работать и как источник тока, и как химический реактор.
Конструкций, в основе которых лежат твёрдые оксидные электролиты, запатентовано очень много, но принцип их действия одинаков и довольно прост. Это пробирка с парой электродов на стенке, снаружи и внутри. Она помещена в нагреватель; внутрь пробирки и в пространство, её окружающее, можно подводить газ. Посмотрим, какие функции могут выполнять такие устройства.
Информация о химии
Самнер (Sumner), Джеймс Бетчеллер
Американский биохимик Джеймс Бетчеллер Самнер родился в Кантоне (штат Массачусетс), неподалеку от Бостона, в семье Элизабет Рэнд (Келли) и Чарльза Самнера, преуспевающего фермера и хозяина хлопкопрядильной фабрики, чьи предки имми ...
Химическая технология
Успехи органической химии стимулировали бурное развитие химической промышленности, прежде всего в Германии. Была разработана технология производства серной кислоты, на основе которой получали взрывчатые вещества, красители и соду, ...
Uup — Ununpentium (Унунпентиум)
Унунпентиум (Унунпентий) (лат. Ununpentium), Uup, химический элемент V группы периодической системы, атомный номер 115, атомная масса [288], наиболее устойчивый изотоп 287Uup. Свойства: радиоактивен. Металл, повидимому находится ...


