Исследование условий возникновения колебательного режима в процессе окислительного карбонилирования фенилацетилена
Рефераты по химии / Исследование условий возникновения колебательного режима в процессе окислительного карбонилирования фенилацетиленаСтраница 12
Еще одним новым направлением научных исследований является изучение особенностей самой реакции Белоусова- Жаботинского или сходных с ней (Бриггса-Раушера, Брея-Либавски и т.п.).
Например,
ранее реакцию Белоусова проводили в закрытом реакционном сосуде, поэтому из-за расходования реагентов (бромата и малоновой кислоты) колебания затухали. Затем в проточном реакторе непрерывного перемешивания получили незатухающие колебания [21], что позволило изучать тонкие стороны механизма автоколебаний, в частности зависимость периода и амплитуды колебаний от интенсивности ультрафиолетового излучения. В таком реакторе был зарегистрирован и режим прерывистой генерации. 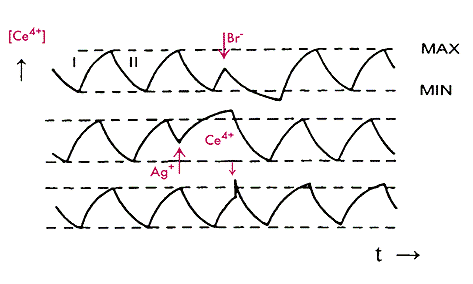 Рис.2.3.3 Автоколебания концентрации церия и принудительная смена стадий I и II, вызываемая добавкой Br-, Ag+ и Ce4+.
Рис.2.3.3 Автоколебания концентрации церия и принудительная смена стадий I и II, вызываемая добавкой Br-, Ag+ и Ce4+.
В системе имеется некоторая концентрация Ce4+. На стадии II образуется Br-, который после взаимодействия с активными частицами реакции окисления Ce3+ исчезает из системы. При достаточно большой концентрации Br- окисление полностью заторможено. Когда концентрация Ce4+ уменьшается и достигает минимального значения, резко падает концентрация Br-. Окисление Ce3+ (I стадия) начинается с большой скоростью, и концентрация Ce4+ возрастает; когда она достигает максимального значения, увеличивается концентрация Br-, что тормозит окисление Ce3+. После этого цикл повторяется. Одновременно измеряя концентрацию йода спектрофотометрически и потенциал йодсеребряного электрода (концентрацию I-), получается классическая картина разрывного предельного цикла в периодической реакции Брея, когда в системе концентрация I2 служит медленной переменной, а концентрация I- - быстрой. Используя спектрофотометрическую запись (Ce4+) одновременно с записью потенциала бромсеребряного электрода (Br-), можно увидеть достаточно сложные фазовые портреты.
В Ивановском Институте растворов РАН в 2001 г. были проведены экспериментальные исследования динамических свойств плазмы в условиях инициирования гетерогенных химических реакций. Было доказано, что химически реагирующая плазма при пониженном давлении проявляет колебательный динамический режим, который влияет на линейный выход продуктов. Можно полагать, что многие известные в настоящее время “гладкопротекающие” сложные реакции могут проходить при определенных концентрационных и температурных условиях в колебательном режиме. В табл.2.3.3. приведены некоторые из найденных гомогенных колебательных окислительно-восстановительных процессов.
Таблица 2.3.3.
Гомогенные окислительно – восстановительные каталитические колебательные процессы [22].
|
Номер процесса |
Наименование |
Окислитель |
Восстановитель |
Катализатор |
|
1 |
Броматные осцилляторы |
HBrO2 |
Карбоновые кислоты, кетоны, фенолы,NaH2PO2,KMnO4 |
Ce(III,IV); Mn(II,III); Cu(II,III)L1; Ni(II,III)L1; Fe(II,III)L2,L3;Co(II,III)L2,L3; Ru(II,III)L2,L3; Os(I,II)L3; Ag(I,II)L3; Cr(I,II)L3 * |
|
2 |
Броматные осцилляторы |
HBrO3 |
Фенолы, альдегиды |
CuIIL1, NiIIL1 |
|
3 |
Иодатные осцилляторы |
HIO2 ,H2O2, |
CH2(COOH)2, S2O32- |
Mn(II) |
|
4 |
Хлоритные осцилляторы |
HClO2 |
I-; S2O32- |
CH2(COOH)2 |
|
5 |
Кислородные осцилляторы |
O2 |
Бензойная кислота |
Co(III,IV) |
Информация о химии
Ричардс (Richards), Теодор Уильям
Американский химик Теодор Уильям Ричардс родился в Джермантауне (штат Пенсильвания), в семье квакеров. Он был четвертым по счету из шести детей в семье преуспевающего художника-мариниста Уильяма Торста Ричардса и поэтессы Анны (Мэ ...
I — Иод
ИОД (йод) (лат. Iodum), I (читается «йод»), химический элемент с атомным номером 53, атомная масса 126,9045. Иод расположен в пятом периоде в группе VIIА периодической системы элементов Менделеева, относится к галоген ...
Биохимия
Эта научная дисциплина, занимающаяся изучением химических свойств биологических веществ, сначала была одним из разделов органической химии. В самостоятельную область она выделилась в последнее десятилетие 19 в. в результате исслед ...


