Реакции ацилирования
Рефераты по химии / Реакции ацилированияСтраница 5
2.5 Ацилирование аминов амидами
Это реакция обмена, и ее обычно проводят с солью амина. Уходящей группой служит, как правило, NH2, а не NHR или NR2; в качестве реагентов наиболее широко применяются первичные амины (в виде солей).
Для образования комплекса с уходящим аммиаком можно добавлять BF3. Эту реакцию часто применяют для получения замещенных производных мочевины из самой мочевины:
Диметилформамид можно превратить в другие формамиды продолжительным нагреванием с первичным или вторичным амином.
3. Реакции O-ацилирования
3.1 Гидролиз ацилгалогенидов
Ацилгалогениды очень реакционноспособны, поэтому гидролиз проходит легко. Большинство галогеноангидридов простых кислот следует хранить в безводных условиях, так как они реагируют с влагой воздуха. Поэтому обычно вода оказывается достаточно сильным нуклеофилом для проведения реакции гидролиза, хотя в отдельных случаях необходимо использовать гидроксид-ион.
Реакция, как правило, не имеет синтетической ценности, так как ацилгалогениды обычно получают из кислот. Реакционная способность ацилгалогенидов изменяется в следующем ряду: F<Cl<Br<I. При использовании в качестве нуклеофила карбоновой кислоты возможна реакция обмена.
Гидролиз галогеноангидридов обычно не катализируется кислотами, за исключением ацилфторидов, когда образование водородной связи может способствовать отщеплению фтора.
3.2 Гидролиз ангидридов
Гидролиз ангидридов можно катализировать основаниями. Конечно, OH-группа атакует более энергично, чем вода, но и другие основания могут катализировать эту реакцию. Это явление, называется нуклеофильным катализом.
3.3 Гидролиз сложных эфиров
Гидролиз сложных эфиров обычно катализируется как кислотами, так и основаниями. Поскольку группа OR обладает более слабыми нуклеофугными свойствами, чем галогены или OCOR, вода не гидролизует большинство сложных эфиров.
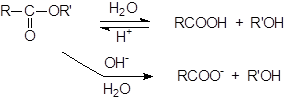 |
При катализе основаниями, атакующей частицей служит более сильный нуклеофил – OH-группа. Эта реакция носит название омыления и приводит к соли кислоты. Кислоты катализируют реакцию за счет того, что положительный заряд атома углерода карбонильной группы становится больше, и, следовательно, он легче подвергается атаке нуклеофилом. Обе реакции обратимы, и поэтому практической ценностью обладают только тогда, когда равновесия удаётся каким либо образом сместить вправо. А поскольку образование соли – один из таких способов, гидролиз сложных эфиров в препаративных целях почти всегда проводят в щелочных растворах, за исключением тех случаев, когда вещество неустойчиво к действию оснований.
Информация о химии
Pu — Плутоний
ПЛУТОНИЙ (лат. Plutonium), Pu, химический элемент III группы периодической системы, атомный номер 94, атомная масса 244,0642, относится к актиноидам. Свойства: серебристо-белый металл; плотность 19,8 г/см3, tпл 640 °С. Радиоа ...
Луллий (Lullius), Раймунд
Философ, богослов, писатель и алхимик Раймунд Луллий родился на о. Мальорка; он принадлежал к знатному и богатому роду и провел свою молодость в роскоши и кутежах при Арагонском дворе. Тридцати лет он оставил жизнь блистательного ...
Биоорганическая химия
Биоорганическая химия — наука, которая изучает связь между строением органических веществ и их биологическими функциями. Объектами изучения являются биологически важные природные и синтетические соединения, такие как биополи ...


