Получение метана и опыты с ним
Рефераты по химии / Получение метана и опыты с нимСтраница 2
Так как в процессе нагревания спирта и серной кислоты кроме этилена получаются другие вещества (SO2, диэтиловый эфир, CO2 и др.), некоторые из которых также могут обесцвечивать раствор KMnO4 и бромную воду, то на пути газовой смеси из пробирки-реактора перед первой U-образной трубкой, следует
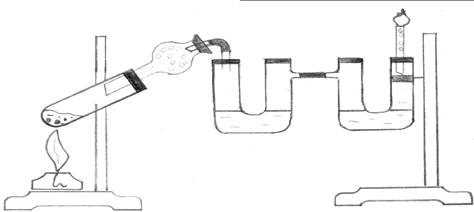
Рис. 2. Получение этилена и опыты с ним.
поместить хлоркальциевую трубку с активированным углем.
Пробирку-реактор нагреть до равномерного кипения. Наблюдать равномерное синхронное пробулькивание воздуха, а затем этилена через раствор KMnO4 и бромную воду. Окраска растворов постепенно исчезает. После полного обесцвечивания растворов поднести пламя спички или горящей лучины к трубке с оттянутым концом и поджечь этилен. Написать уравнения реакций, объяснить наблюдаемые явления.
Техника безопасности. Поджигать этилен после полного обесцвечивания раствора KMnO4 и бромной воды. Прибор должен быть герметичным, что определяется синхронным пробулькиванием газа через растворы KMnO4 и бромной воды.
Утилизация. Вследствие окисления спирта в пробирке-реакторе остается обуглившаяся смесь неопределенного состава, которую полностью переносят в емкость-нейтрализатор. В раствор, оставшийся после обесцвечивания перманганата калия, добавить немного крепкого подкисленного H2SO4 раствора KMnO4 и прокипятить. Все имеющиеся органические соединения окисляются до углекислого газа и воды:
Cх Hу Oz + KMnO4 + H2SO4 → MnSO4 + K2SO4 + CO2 + H2O.
Раствор KMnO4 использовать многократно. Утилизацию полученного MnSO4 (после отработки раствора) см.: VIII кл., тема "Галогены". В раствор, оставшийся после обесцвечивания бромной воды, добавить небольшую порцию железного порошка и несколько капель соляной кислоты средней концентрации:
Fe + HCI = FeCI2 + 2H.
Через некоторое время бромпроизводные восстановятся атомарным водородом до углеводородов и бромид-ионов, к примеру, по схеме:
C2H4Br2 + 2H = C2H6 + 2HBr (FeBr2).
Далее добавить несколько капель хлорной воды:
2FeBr2 + 3CI2 = 2FeCI3 + 2Br2.
Полученный раствор имеет желтовато-бурый цвет бромной воды, который можно использовать для определения непредельных углеводородов и демонстрации окислительных свойств брома. Далее фильтрованием отделяют железный порошок, который промывают, сушат и используют вновь.
ЛАБОРАТОРНАЯ РАБОТА № 2
Опыт 1. Получение этилена дегидратацией этанола над оксидом алюминия
Описанный выше опыт получения этилена дегидратацией этанола в присутствии H2SO4 (конц) приводит к образованию большого количества оксида серы (IV) и множества других токсичных соединений, опасных для окружающей среды. Оксид серы (IV) очень быстро обесцвечивает раствор KMnO4 и бромную воду, что делает некорректным описанный опыт в целях учебной демонстрации: C2H5OH + 2H2SO4 = 2C+2SO2 + 5H2O, далее:
C + 2H2SO4 = CO2 + 2SO2 + 2H2O (при нагревании)
5SO2+2KMnO4+2H2O = K2SO4+2MnSO4+2H2SO4
SO2+Br2+2H2O = H2SO4+2HBr
Более простой и экологически чистый вариант получения этилена основан на пропускании паров спирта над нагретым твердым катализатором из оксида алюминия.
Оборудование и реактивы: Демонстрационная круглодонная пробирка, стеклянные и резиновые газоотводные трубки, две U-образные трубки, пробирки, стеклянная трубка с оттянутым концом, штатив, лапка штатива, спиртовка, лучинка, этанол, промытый и прокаленный песок, катализатор из глины в смеси с оксидом аллюминия, вода дистиллированная.
Информация о химии
Структурная химия
В 1857 Кекуле, исходя из теории валентности (под валентностью понималось число атомов водорода, вступающих в соединение с одним атомом данного элемента), предположил, что углерод четырехвалентен и потому может соединяться с четырь ...
Агрикола (Agricola), Георг
24 марта 1490 г. – 21 ноября 1555 г. Георг АгриколаНемецкий учёный в области горного дела и металлургии Георг Агрикола [настоящая фамилия Бауэр (Bauer); лат. agricola – земледелец, перевод немецкого слова Bauer] родил ...
Таубе (Taube), Генри
Канадо-американский химик Генри Таубе родился в Ньюдорфе (провинция Саскачеван, Канада), в семье Альбертины (Тайдетски) Таубе и Самюэла Таубе. Окончив местную школу, он поступил в Саскачеванский университет, где в 1935 г. получил ...


