Производство неконцентрированной азотной кислоты
Рефераты по химии / Производство неконцентрированной азотной кислотыСтраница 22
2)Тепло окисления монооксида азота в диоксид:
Q2= 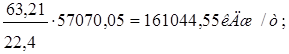
где 57070,05- теплота окисления монооксида азота в диоксид, кДж/кмоль;
3)Тепло образования моногидрата:
Q3= 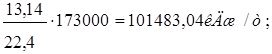
где 173000-теплота образования азотной кислоты, кДж/кмоль;
13,14-количество сконденсировавшихся паров воды, кг/т;
4)Тепло разбавления моногидрата:
Q4= 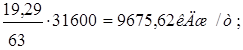
где 19,29-количество растворенного моногидрата азотной кислоты,кг;
31600-теплота разбавления моногидрата кислоты, кДж/кмоль;
5)Тепло конденсации воды:
Q5=![]() ;
;
Где 4939,6-тепло конденсации воды, кДж/кмоль;
Общий приход тепла: ![]() Q=1593275,84кДж/т;
Q=1593275,84кДж/т;
Расход тепла:
Рассчитаем теплоемкости компонентов газовой смеси на выходе в холодильник-конденсатор при температуре 55![]() или 328К.
или 328К.
Теплоемкость кислорода:
Теплоемкость азота:
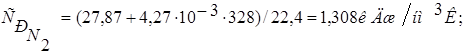
Теплоемкость воды:
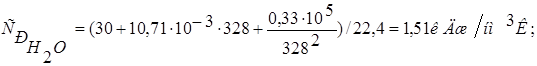
Теплоемкость оксида азота (II):
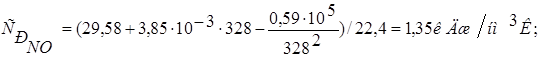
Теплоемкость оксида азота (IV):
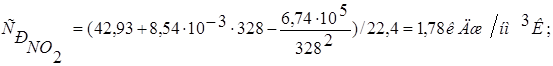
Средняя теплоемкость нитрозного газа на выходе из аппарата:
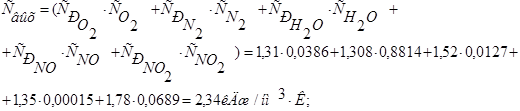
1)Тепло, уходящее с нитрозным газом:
Q1’= ![]() =
= ![]()
где ![]() - температура нитрозного газа на выходе из холодильника, 0С ;
- температура нитрозного газа на выходе из холодильника, 0С ;
2)Тепло, уходящее с кислотой:
Q2’ =mk ![]() Ck
Ck ![]() tk =
tk =![]() где
где
mk-масса кислоты, кг/т;
Ck-теплоемкость кислоты, кДж/кмоль;
tk- температура кислоты,![]()
3) Теплопотери:
Принимаем, что потери тепла в окружающую среду составляют 3% от общего количества, поступающего в аппарат.
Q3’=![]()
4)Тепло отводимое с охлаждающей водой;
Q4’= ![]() Q-( Q1’+ Q2’+ Q3’)=
Q-( Q1’+ Q2’+ Q3’)=
![]() ;
;
Таблица 3.3.2.1
Тепловой баланс холодильника-конденсатора.
|
Статьи прихода |
кДж/т |
% |
Статьи расхода |
кДж/т |
% |
|
1) Тепло с газами |
670122,29 |
42,05 |
1)Тепло с газами |
483545,21 |
30,34 |
|
2) Тепло окисления |
161044,55 |
10,11 |
2)Тепло с кислотой |
3085,24 |
0,19 |
|
3) Тепло образования моногидрата |
101483,04 |
6,37 |
3)Теплопотери |
47798,27 |
2,99 |
|
4) Тепло разбавления моногидрата |
9675,62 |
0,61 |
4)Тепло, уходящее с водой |
1058847,12 |
66,46 |
|
5) Тепло конденсации воды |
650950,34 |
40,86 | |||
|
Итого: |
1593275,84 |
100 |
Итого: |
1593275,84 |
100 |
Информация о химии
Гиббс (Gibbs), Джозайя Уиллард
Американский физик и математик Джозайя Уиллард Гиббс родился в Нью-Хейвене, штат Коннектикут. Он окончил Йельский университет, где его успехи в греческом, латыни и математике были отмечены призами и премиями. В 1863 г. Гиббс получ ...
Шталь (Stahl), Георг Эрнст
Немецкий врач и химик, создатель теории флогистона Георг Эрнст Шталь родился 21 октября 1660 (по другим данным – 1659 г.) в Ансбахе. В 1673–1679 гг. он изучал медицину и химию в Йенском университете, после окончания ко ...
Химия полимеров
Химия полимеров — раздел химии, в котором изучаются химические свойства полимеров. Делится на разделы: физическая химия полимеров, структурная и т. д. Синоним — химия высокомолекулярных соединений — раздел орган ...


