Общие сведения по давлению паров
Рефераты по химии / Понятие давления паров и теплоты / Общие сведения по давлению паров
Согласно правилу фаз, давление паров чистой жидкости является однозначной функцией температуры насыщения, поэтому почти все данные о давлении паров представляют в виде зависимости
![]() .(7.1)
.(7.1)
Давление насыщенного пара ![]() может быть связано с любым другим интенсивным свойством насыщенной жидкости (или пара), однако температура насыщения в этом случае наиболее удобна. Если паровая фаза находится в равновесии с жидкой фазой, то условие равенства химических потенциалов, температуры и давления обеих фаз приводит к уравнению Клаузиуса-Клапейрона:
может быть связано с любым другим интенсивным свойством насыщенной жидкости (или пара), однако температура насыщения в этом случае наиболее удобна. Если паровая фаза находится в равновесии с жидкой фазой, то условие равенства химических потенциалов, температуры и давления обеих фаз приводит к уравнению Клаузиуса-Клапейрона:
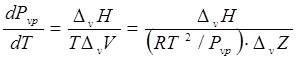 (7.2)
(7.2)
или
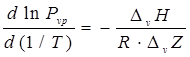 .(7.3)
.(7.3)
Большинство уравнений для расчета и корреляции давления паров получаются путем интегрирования уравнения (7.3). После интегрирования должна быть выбрана форма зависимости группы ![]() от температуры, а константа интегрирования определяется по одной точке “давление паров -температура”.
от температуры, а константа интегрирования определяется по одной точке “давление паров -температура”.
В общем случае зависимость ![]() от
от ![]() имеет S-образный вид. Для большинства веществ изменение наклона соответствует значению приведенной температуры
имеет S-образный вид. Для большинства веществ изменение наклона соответствует значению приведенной температуры ![]() =0,8-0,85. Для низкокипящих или неполярных соединений эта величина имеет более низкое значение (для метана точка перегиба
=0,8-0,85. Для низкокипящих или неполярных соединений эта величина имеет более низкое значение (для метана точка перегиба ![]() =0,7), для высококипящих, а также для полярных или ассоциированных жидкостей точка перегиба перемещается в область более высоких значений Tr (для этанола – 1,0).
=0,7), для высококипящих, а также для полярных или ассоциированных жидкостей точка перегиба перемещается в область более высоких значений Tr (для этанола – 1,0).
S-образный вид зависимости ![]() от
от ![]() обусловлен изменением отношения
обусловлен изменением отношения ![]() с температурой. Для нормальных жидкостей это отношение сравнительно нечувствительно к изменению температуры в диапазоне между нормальной температурой кипения вещества и его критической температурой. Объясняется это тем, что уменьшение теплоты парообразования компенсируется в некоторой степени уменьшением величины
с температурой. Для нормальных жидкостей это отношение сравнительно нечувствительно к изменению температуры в диапазоне между нормальной температурой кипения вещества и его критической температурой. Объясняется это тем, что уменьшение теплоты парообразования компенсируется в некоторой степени уменьшением величины ![]() . Ниже нормальной точки кипения (при
. Ниже нормальной точки кипения (при ![]() = 0,6-0,7) значение
= 0,6-0,7) значение ![]() очень близко к единице и изменение отношения
очень близко к единице и изменение отношения ![]() происходит исключительно вследствие изменения энтальпии.
происходит исключительно вследствие изменения энтальпии.
Информация о химии
Нобелевка по химии присуждена за открытие квазикристаллов
Шведская королевская академия наук решила присудить Нобелевскую премию по химии Дэниелу Шехтману (Dan Shechtman), профессору Израильского технологического института (Technion). Химик удостоен награды за открытие квазикристаллов ( ...
Самнер (Sumner), Джеймс Бетчеллер
Американский биохимик Джеймс Бетчеллер Самнер родился в Кантоне (штат Массачусетс), неподалеку от Бостона, в семье Элизабет Рэнд (Келли) и Чарльза Самнера, преуспевающего фермера и хозяина хлопкопрядильной фабрики, чьи предки имми ...
Белки и полипептиды
Белки играют исключительно важную роль в живой природе. Жизнь немыслима без различных по строению и функциям белков. Белки - это биополимеры сложного строения, макромолекулы (протеины) которых, состоят из остатков амин ...


