Методы защиты металлов от коррозии
Рефераты по химии / Теоретические основы электрохимической коррозии / Методы защиты металлов от коррозииСтраница 1
В зависимости от характера коррозии и условий ее протекания применяются различные методы защиты. Выбор того или иного способа определяется его эффективностью в данном конкретном случае, а также экономической целесообразностью. Любой метод защиты изменяет ход коррозийного процесса, уменьшая скорость или прекращая его полностью. Поляризационные или коррозионные диаграммы, наиболее полно характеризующие коррозионный процесс, должны отражать и те изменения в ходе его протекания, какие наблюдаются в условиях защиты. Поляризационные диаграммы можно использовать поэтому при разработке возможных путей предохранения металлов от коррозии. Они служат основой при выяснении принципиальных особенностей того или иного метода. В связи с этим при рассмотрении существующих методов защиты будем пользоваться поляризационными диаграммами в их несколько упрощенном виде (рисунок 6). На таких диаграммах постулируется линейная зависимость между плотностью тока и потенциалом каждой частной реакции. Это упрощение оказывается вполне допустимым при качественной оценке особенностей большинства методов защиты.
Эффективность защиты выражают при помощи коэффициента торможения у или степени защиты Z.
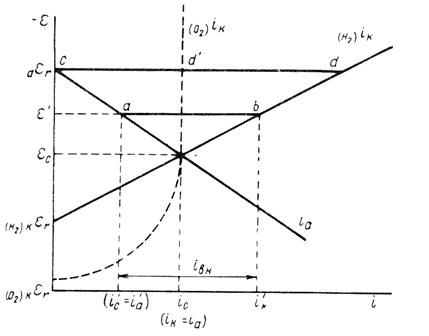
Рисунок 6 - Упрощенная поляризационная диаграмма коррозионного процесса, протекающего с водородной деполяризацией
Коэффициент торможения показывает, во сколько раз уменьшается скорость коррозии в результате применения данного способа защиты (уравнение 16).
ϒ = ic/i׳c (16)
где ic и i׳c — скорость коррозии до и после защиты. Степень защиты указывает, насколько полно удалось подавить коррозию благодаря применению этого метода (уравнения 17 и 18).
Z = (ic - i׳c)/ ic (17)
или
Z% = (ic - i׳c) 100/ ic (18)
Все методы защиты условно делятся на следующие группы:
- электрические методы;
- методы, связанные с изменением свойств корродирующего металла;
- методы, связанные с изменением свойств коррозионной среды;
- комбинированные методы.
Электрические методы защиты основаны на изменении электрохимических свойств металла под действием поляризующего тока. Наибольшее распространение получила защита металлов при наложении на них катодной поляризации. При смещении потенциала металла в сторону более электроотрицательных значений (по сравнению с величиной стационарного потенциала коррозии) скорость катодной реакции увеличивается, а скорость анодной падает (рисунок 6). Если при εс соблюдалось равенство
ik =ia, то при более отрицательном значении ε' это равенство нарушается -
i׳k ≠i׳a, причем i׳k>i׳a.
Уменьшение скорости анодной реакции при катодной поляризации эквивалентно уменьшению скорости коррозии. Коэффициент торможения при выбранном потенциале ε' (рисунок 4) будет
ϒ = ic/i׳c = ic/i׳а = ic/0,5iс= 2,
а степень защиты достигает 50%:
Z = (ic - i׳c) 100/ ic = (ic – i׳а) 100/ ic = (ic – 0,5ic) 100/ ic =50%
Внешний ток iвн , необходимый для смещения потенциала до значения ε', представляет собой разницу между катодным и анодным токами:
iвн = i׳к – i׳а;
его величина на рисунке 6 выражается прямой ab. По мере увеличения внешнего тока потенциал смещается в более отрицательную сторону и скорость коррозии должна непрерывно падать. Когда потенциал корродирующего металла достигает равновесного потенциала анодного процесса аεг, скорость коррозии сделается равной нулю ( ic = iа = 0), коэффициент торможения - бесконечности, а степень защиты - 100%. Плотность тока, обеспечивающая полную катодную защиту, называется защитным током iз. Его величине на рисунке 6 соответствует отрезок cd. Величина защитного тока не зависит от особенностей протекания данной анодной реакции, в частности от величины сопровождающей ее поляризации, а целиком определяется катодной поляризационной кривой. Так, например, при переходе от водородной к кислородной деполяризации сила защитного тока уменьшается и становится равной предельному диффузионному току (отрезок cd' на рисунке 6).
Информация о химии
Rb — Рубидий
РУБИДИЙ (лат. Rubidium), Rb, химический элемент I группы периодической системы Менделеева, атомный номер 37, атомная масса 85,4678. Относится к щелочным металлам. Свойства: серебристо-белый металл пастообразной консистенции. Плот ...
Белки и полипептиды
Белки играют исключительно важную роль в живой природе. Жизнь немыслима без различных по строению и функциям белков. Белки - это биополимеры сложного строения, макромолекулы (протеины) которых, состоят из остатков амин ...
Шееле (Scheele), Карл Вильгельм
Шведский химик Карл Вильгельм Шееле родился в Штральзунде в Померании, которая тогда входила в состав Швеции, в семье пивовара и торговца зерном. Шееле учился в частной школе в Штральзунде, но уже в 1757 г. переехал в Гётеборг. По ...


