Теория активированного комплекса (ТАК)
Рефераты по химии / Теория активированного комплекса (ТАК)Страница 1
Теория Активированного Комплекса –Теория Переходного Состояния - Теория Абсолютных Скоростей химических реакций . Всё это наименования одной и той же теории, в которую ещё в 30-е годы оформились попытки представить процесс активации с помощью и достаточно детальных, и вместе с тем всё же достаточно общих, моделей, построенных на базе статистической механики и квантовой химии (квантовой механики), комбинируя их и создавая иллюзию индивидуального анализа конкретного химического превращения уже на стадии перестройки электронно-ядерной структуры реагентов.
Сама задача кажется очень сложной, и поэтому в ТАК неизбежно образовалось довольно много логических неясностей . Всё же это наиболее общая и плодотворная из теоретических концепций, посредством которых в настоящее время описывают элементарные процессы, и её возможности не ограничены рамками лишь химического элементарного акта. С нею оказалось тесно связано развитие современной химической кинетики. К ней привязаны новейшие алгоритмы и графические приёмы компьютерной химии, и на её основе быстро развивается орбитальная теория химической реакционной способности .
И это далеко не всё! На основе ТАК оказалось возможно единообразно проанализировать множество физико-химических явлений и многих макроскопических свойств веществ, что, на первый взгляд, выглядят уделом лишь научной эмпирики, казалось бы безнадёжно недоступной для теоретического осмысления. Ряд таких ситуаций читатель найдёт в великолепной, хотя и давней, книге Глесстона, Эйринга и Лейдлера “Теория абсолютных скоростей”, написанной творцами этой теории .
В качестве элементарных реакций в газовой фазе тримолекулярные соударения не являются распространёнными, поскольку даже в хаотических броуновских движениях очень мала вероятность одновременных столкновений трёх частиц. Вероятность тримолекулярной стадии резко возрастает, если она протекает на границе раздела фаз, и фрагменты поверхности конденсированной фазы оказываются её участниками. За счёт подобных реакций часто создаётся основной канал изъятия у активных частиц избыточной энергии и их исчезновения в сложных превращениях.
Рассмотрим тримолекулярное превращение вида: ![]()
Из-за малой вероятности тримолекулярных соударений целесообразно ввести более реалистичную схему, использующую симметризованный набор бимолекулярных актов. (см. Эмануэль и Кнорре, стр. 88-89.)
Качественная модель последовательных бимолекулярных соударений:
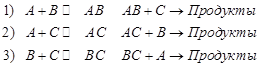
Основное допущение основано на детальном равновесии на первой стадии:
Квазиравновесный режим образования бимолекулярных комплексов
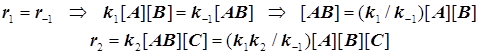
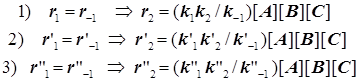
![]()
![]()
Результирующая константа скорости должна принять вид:
![]() (7.1)
(7.1)
Рассмотрим элементарные положения теории активированного комплекса, включая:
- кинетическую схему активации через промежуточное переходное состояние,
- квазитермодинамику активации через образование активированного комплекса,
- размерность константы скорости реакции второго порядка в ТАК.
Простейшая кинетическая модель активации в ТАК:
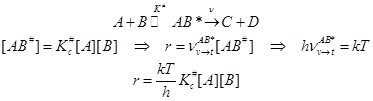 (6.1)
(6.1)
Первая стадия механизма активации бимолекулярная. Она обратимая, на ней образуется активированный комплекс, а он далее распадается по двум маршрутам: а) обратно в реагенты, с которыми он находится в равновесии, и для этого процесса следует ввести константу равновесия, б) в продукты реакции и этот финальный процесс характеризуется некоторой механической частотой распада. Сочетая эти стадии, несложно рассчитать константу скорости реакции. Удобно рассматривать превращение в газовой фазе.
Константа равновесия обратимой стадии может быть выражена следующим способом.
Если стандартные состояния в газовой фазе выбраны согласно обычному термодинамическому правилу, и стандартизованы парциальные давления газообразных участников реакции, то это означает:
Информация о химии
Гебер (Geber) – Джабир ибн Хайан
Арабский учёный Абу Муса Джабир ибн Хайян (латинизированное имя – Гебер) родился в г. Туси, провинция Хорасан, Иран, в семье аптекаря Хайана аль Азди, происходившего из Йемена. Сведения о жизни и деятельности Джабира ибн Хай ...
Уилкинс (Wilkins), Морис Хьюг Фредерик
Английский биофизик Морис Хьюг Фредерик Уилкинс родился в Понгароа (Новая Зеландия). Его мать, Эвелин (Виттейкер) Уилкинс, эмигрировала из Ирландии. Отца, Эдгара Генри Уилкинса, школьного доктора, очень привлекала исследовательска ...
Бройль (de Broglie), Луи Виктор Пьер Раймон де
Французский физик Луи Виктор Пьер Раймон де Бройль родился в Дьеппе. Он был младшим из трех детей Виктора де Бройля и урожденной Полин де ля Форест д'Армайль. Как старший мужчина этой аристократической семьи, его отец носил титул ...


