Физико-химические свойства водных растворов азотной кислоты
Рефераты по химии / Физико-химические свойства водных растворов азотной кислоты / Физико-химические свойства водных растворов азотной кислотыСтраница 2
Как следует из данных табл. 1 и приведенных на рис. 5 и 6 при кипении раствора, содержащего менее 68,4% HN03, в паровой фазе будет находиться больше паров воды и меньше паров азотной кислоты. Если концентрация азотной кислоты в растворе выше 68,4%, то при кипении в паровой фазе будет больше паров азотной кислоты, чем воды. Таким образом, при ректификации азотной кислоты выше азеотропного состава в дистилляте будет получено концентрированная HN03, а кубовом отходе 68,4%-ная HN03.
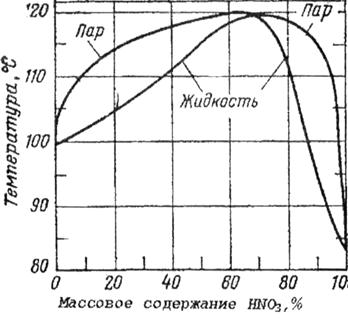
Рис. 5 - Зависимость температуры кипения и массового содержания HNO3 в паровой фазе от массового содержания HNO3 в жидкой фазе при атмосферном давлении
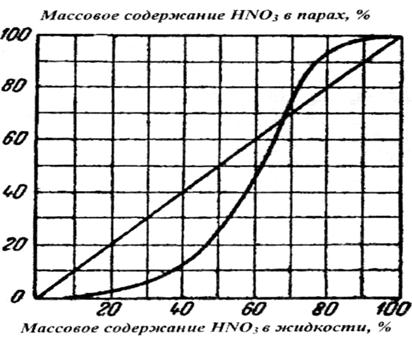
Рис. 6 - Зависимость состава паровой фазы от состава жидкой фазы в системе HN03 – Н20 при атмосферном давлении
Изменение давления при ректификации водного раствора азотной кислоты практически не влияет на соотношение составов паровой и жидкой фаз. Из табл. 2 видно, что при повышении давления от 15,0 до 101,3 кПа состав азеотропной смеси изменяется от 66,8% до 68,4% HNO3.
Таблица 2 - Влияние давления на температуру кипения и состав азеотропной смеси HNO3 - Н20
|
Давление, кПа |
15,0 |
48,0 |
98,0 |
101,3 |
|
Температура, °С |
74,2 |
89,9 |
120,5 |
121,7 |
|
Массовое содержание HN03, % |
66,80 |
67,15 |
68,0 |
68,4 |
Физико-химические свойства системы HN03 - Н20, которые могут быть использованы при инженерных расчетах или в научной практике, приведены на рис. 7 -11 и в табл. 3- 4.
Теплоты разбавления азотной кислоты различной концентрации (0-100% HN03) представлены на рис.7.
Различают интегральную и дифференциальную теплоты растворения.
Интегральная теплота растворения - количество тепла, выделенное при растворении 1 кг-моль вещества в n кг-моль растворителя, с образованием раствора с молярным содержанием вещества X = 1/1+n. Выражают интегральную теплоту растворения в ккал/кг раствора.
Дифференциальная теплота растворения - количество тепла, выделяющегося при растворении 1 кг-моль вещества в бесконечно большом количестве раствора состава X = 1/1+n. Выражают дифференциальную теплоту растворения в ккал/кг растворенного вещества (или на моль-вещества).
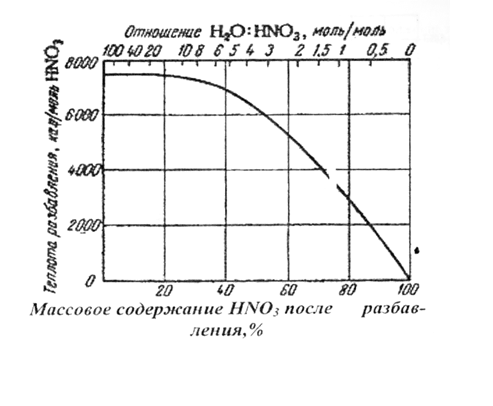
Рис. 7 - Зависимость теплоты разбавления азотной кислоты водой от массового содержания HN03в растворе после разбавления
Теплоту растворения HNO3 в воде определяют по формуле:
Q = ![]() (1.17)
(1.17)
Информация о химии
Создан материал с рекордной фосфоресценцией
Всего через минуту пребывания на солнце новый состав целых две недели довольно ощутимо светится в ближнем инфракрасном диапазоне. Фосфоресцентные материалы, выдающие видимое излучение после «накачки» светом, широко ра ...
Наночастицы позволят разобраться с термитами
Исследователи из Австралии обнаружили, что мезопористые наночастицы оксида кремния [mesoporous silica nanoparticles (MSN)] могут служить хранилищем и способом контролируемой доставки биоцидов. Такой способ доставки биологически ак ...
Sc — Скандий
СКАНДИЙ (лат. Scandium), Sc, химический элемент III группы периодической системы, атомный номер 21, атомная масса 44,95591, относится к редкоземельным элементам. Свойства: плотность 3,02 г/см3, tпл 1541°С. Название: назван о ...


