Получение молибдена из отходов промышленности
Рефераты по химии / Получение молибдена из отходов промышленностиСтраница 15
Первичная обработка в окисляющих растворах может быть применена для любых концентратов. Растворы, полученные после окислительного выщелачивания концентратов, очищают от примесей, после чего из них выделяют необходимые соединения молибдена и рения. Из полученных растворов чистые молибденовые и рениевые соединения могут быть селективно выделены ионообменом или экстракцией.
3.2 Получение парамолибдата аммония (NH4)6Mo7O24 × 4H2O
Химическую переработку «огарков» после обжига богатых высококачественных концентратов производят с целью получения чистых соединений молибдена – парамолибдата аммония и молибденового ангидрида [20, 23]. Из этих последних в случае необходимости легко получить любые другие соединения, в том числе и соединения высокой чистоты. Молибденовый ангидрид, находящийся в огарке, растворяется в растворах аммиака, щелочей, соды, некоторых кислот. Но щелочные металлы – нежелательные примеси для соединений молибдена, применяемых в электротехнической и химической промышленности. В щелочах, соде и кислотах растворяется большое число и других примесей.
Раствор аммиака обладает тем преимуществом, что в нем не растворимо большинство примесей, сопутствующих молибдену в огарке. Поэтому аммиачный способ переработки богатых молибденовых огарков более распространен. Его преимуществами, помимо высокого извлечения МоО3 в раствор и достаточно полного отделения примесей, являются простота дальнейшей очистки аммиачного раствора, легкость выделения молибдена в виде чистого парамолибдата аммония, простота подбора материала для аппаратуры. Схема аммиачного метода переработки огарков после обжига молибденита представлена на рис.3
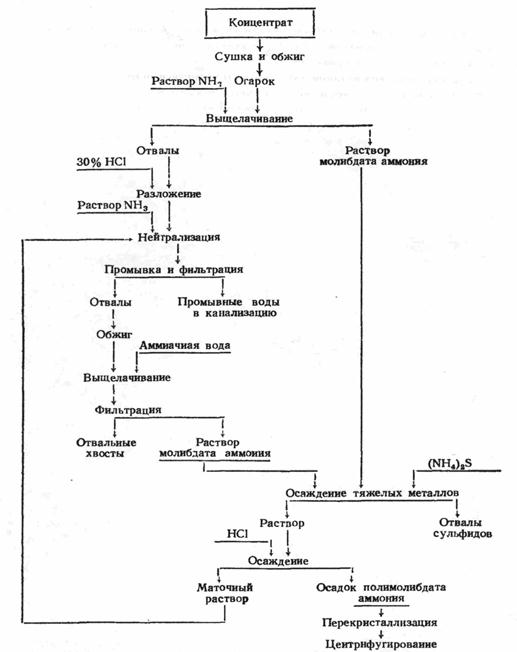
Рис. 3. Cхема переработки огарков с кислотным разложение хвостов выщелачивания
Перед обработкой раствором аммиака рекомендуется промывать огарок водой для удаления растворимых в воде сульфатов (CuSO4, части CaSO4 и др.) и солей щелочных металлов. Но так как при этом несколько теряется молибден, то промывают не всегда. Потеря молибдена при промывке достигает 4 – 5% [20].
При обработке огарка аммиаком происходят реакции:
MoO2 + 2NH4OH = (NH4 )2МоО3 +H2О
CuO + 4NH4OH = [Cu(NH3)4](OH)2 + 3H2O
CuMoO4 + 6NH4OH = [Cu (NH3)4] (OH)2 + (NH4)2 MoO4 + 4H2О
ZnMoO4 + 6NH4OH = (NH4)2 MoO4 + [Zn (NH3)4] (OH)2 + 4H2O NiMoO4 + 6NH4OH = (NH4)2 MoO4 + [Ni (NH3)4] (0H)2 + 4H2O
Аналогично молибдатам реагируют сульфаты меди, цинка, никеля и железа, если они образовались при обжиге. Железо (II) (в составе сульфата или окиси) частично реагирует по уравнению
FeSO4 + 4NH4OH → [Fe (NH3)4] SO4 + 4H2О
и переходит в раствор в составе комплекса. Железо (III), образующееся в результате окисления Fe2+ кислородом воздуха при обжиге и выщелачивании, частично остается в составе химически стойкого Fe3O4, частично дает нерастворимую гидроокись Fe(OH)3.
Остаются без изменения МоО2, СаМоО4, кварц, неокислившиеся при обжиге сульфиды. В аммиачные растворы в зависимости от минералогического состава концентрата и условий обжига переходит 80 – 95% молибдена. Для более полного перевода молибдена в раствор добавляют 60 – 80 кг (NH4)2CO3 на 1 т огарка. Влияние карбоната аммония на извлечение молибдена связано со следующими реакциями:
Информация о химии
Жерар (Gerhardt), Шарль Фредерик
Французский химик Шарль Фредерик Жерар родился в Страсбурге в семье банковского служащего. Окончив протестантскую семинарию в возрасте 15 лет, поступил в Политехническое училище в Карлсруэ. В 1833 г. продолжил образование в Высшей ...
Uup — Ununpentium (Унунпентиум)
Унунпентиум (Унунпентий) (лат. Ununpentium), Uup, химический элемент V группы периодической системы, атомный номер 115, атомная масса [288], наиболее устойчивый изотоп 287Uup. Свойства: радиоактивен. Металл, повидимому находится ...
Специальные варианты высокоэффективной жидкостной хроматографии
...


