Одно- и многоатомные спирты
Рефераты по химии / Одно- и многоатомные спиртыСтраница 2
CH3-OH + HNO3 ¨ CH3-ONO2 + H2O
CH3CH2OH + H2SO4 ® CH3CH2OSO3H + H2O
CH3CH2OH + (CH3CO)2O ® CH3COOC2H5 + CH3COOH
Это – реакции замещения водорода на кислотный остаток.
2. Замещение гидроксильной группы на галоген.
CH3CH2OH + HBr « CH3CH2Br + H2O
Реакция протекает по механизму нуклеофильного замещения.
CH3CH2-OH + SOCl2 ® CH3CH2-Cl + SO2+ HCl
3CH3CH2-OH + PCl3 ® 3CH3CH2-Cl + H3PO4
Ниже приводится механизм взаимодействия спирта с тионилхлоридом:
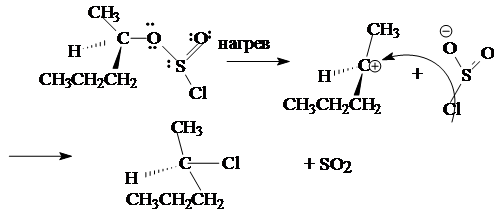
Этот механизм обозначается символом Sni (замещение нуклеофильное внутримолекулярное).
Реакции отщепления
CH3CH2OH ® CH2=CH2
В качестве катализаторов используют минеральные кислоты (серная, фосфорная), кислые соли (KHSO4), ангидриды кислот (Р2О5), оксид алюминия и т.д.
R-OH + R’-OH ® ROR (ROR’, R’OR’) + H2O
Порядок отщепления воды в большинстве случаев определяется
правилом зайцева
: при отщеплении воды наиболее легко отщепляет водород от соседнего наименее гидрированного атома углерода.
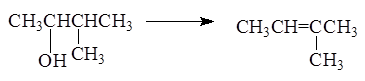
Реакция отщепления воды от спиртов протекает через стадию образования карбкатиона:
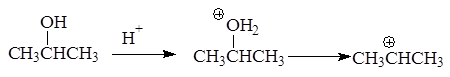
В зависимости от строения спирта образуются первичные, вторичные и третичные карбкатионы:
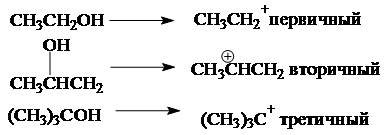
По увеличению стабильности катионы располагаются в следующий ряд: CH3CH2+ < CH3CH+CH3 < (CH3)3C+
Любое влияние, делокализующее положительный заряд карбкатиона, ведет к его стабилизации. Мы имеем дело в данном ряду с индукционной стабилизацией:
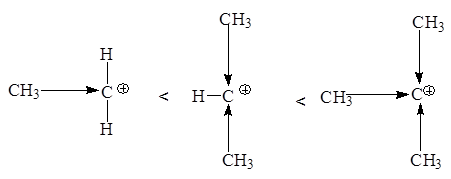
Образующиеся катионы в зависимости от их строения способны к перегруппировкам:
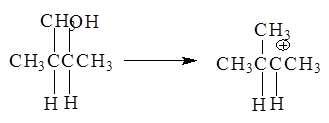
3-Метил-2-бутанол - в 2-метил-2-бутильный катион, склонный к перегруппировке в более стабильный:
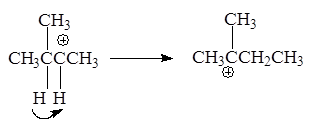
Образование последнего 2-метил-2-бутильного катиона связано с гидридным перемещением (Н-) из положения 3 в положение 2.
В перегруппировке может участвовать и алкильная группа:
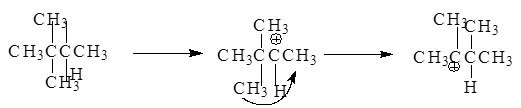
Основное различие между тремя типами реакционных интермедиатов (карбкатионы, карбанионы и свободные радикалы) состоит в том, что карбкатионы имеют тенденцию изомеризоваться в более устойчивые частицы.
Окисление. Первичные и вторичные спирты могут быть окислены соответственно до альдегидов и кетонов. Третичные спирты устойчивы к окислению в мягких условиях.
Первичные спирты окисляются до альдегидов под действием окислителей, содержащих Cr(VI). Это обычно хромовая кислота H2CrO4:
R-CH2-OH + H2CrO4 ® R-CHO + H2CrO3 (неустойчива) + H20
Окисление первичного спирта начинается с образования эфира хромовой кислоты RCH2-O-Cr(O)2-OH. На следующей стадии эфир претерпевает реакцию отщепления, в результате которой образуется двойная связь С=О.
Альдегиды можно также получить окислением первичных спиртов реагентом Саретта (комплекс CrO3 с пиридином).
В относительно мягких условиях происходит окисление спирта разбавленным раствором оксида хрома (VI) в разбавленной серной кислоте (окисление по Джонсу).
Вторичные спирты легко окисляются до кетонов под действием K2Cr2O7+H2SO4+H20 , CrO3+CH3COOH+H2O и KMnO4 в кислой среде:
(R )2CH-OH + [O] ® R-CO-R + H2O
Механизм окисления вторичных спиртов подобен окислению первичных спиртов в альдегиды, поэтому для получения кетонов пригодны методы, описанные выше.
Дегидрирование спиртов. Этим способом получают многие альдегиды и кетоны:
2R-CH2-OH ® R-COH + H2
2(R)2-CH-OH ® (R)2-CO + H2
В качестве катализатора используются металлическая медь и серебро. В промышленности этот процесс реализован для получения формальдегида из метанола.
Многоатомные спирты
Обычно названия двухатомных спиртов производятся от названия двухатомного радикала с прибавлением слова гликоль, например этиленгликоль, пропиленгликоль. По Женевской номенклатуре пользуются окончанием -ол, но указывают число гидроксильных групп - диол, -триол, -тетрол и т.д.
В двухатомных спиртах гидроксилы могут быть соединены с первичными, вторичными и третичными атомами углерода, поэтому различают гликоли двупервичные, первично-вторичные и т.д.
Синтез гликолей осуществляется в основном теми же способами, что одноатомных спиртов, кроме того, окислением соответствующих алкенов перманганатом калия в щелочной среде (реакция Вагнера)
Информация о химии
Ta — Тантал
ТАНТАЛ (лат. Tantalum), Та, химический элемент V группы периодической системы, атомный номер 73, атомная масса 180,9479. Свойства: светло-серый с синеватым отливом металл, тяжелый и тугоплавкий; плотность 16,6 г/см3, tпл 3014 &de ...
Разес (Rhazes) – Абу Бакр Мухаммед ибн Закарийа Ар-Рази
Иранский учёный-энциклопедист, врач, алхимик и философ Абу Бакр Мухаммед ибн Закария Ар-Рази (латинизированное имя Разес, Rhazes) родился в персидском городе Рее, близ Тегерана. В Персии, а также в городах, расположенных на террит ...
Зоман
Синонимы: EA 1210 GD soman метилфторфосфоновой кислоты пинаколиловый эфир Внешний вид: бесцветн. жидкость Брутто-формула (система Хилла): C7H16FO2P CAS №: 96-64-0 Молекулярная масса (в а.е.м.): 182,17 Температура плавл ...


