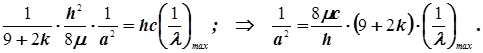Электронные спектры поглощения. Электронные спектры красителей и модель одномерного ящика.
Рефераты по химии / Молекулярные спектры / Электронные спектры поглощения. Электронные спектры
красителей и модель одномерного ящика.Страница 3
Номер граничного уровня -ВЗМО равен числу электронных пар – числу двойных связей. В кольцах и вне полиенового мостика это число равно 4 и в полиеновом мостике ещё k и всего получаем число -электронных пар (4+k), это же есть и номер ВЗМО (4+k) (см. структурную формулу). Номер m уровня НВМО, на которую при возбуждении переходит электрон, на 1 больше, и равен m=n+1=4+k+1=5+k.
То же самое число (4+k) равно количеству чередующихся фрагментов с двойной и одинарной связью типа C=C-C между двумя атомами N. Длина фрагмента N+=C-C (или N -C=C) в циклах считается равной C =C-C. Если усреднённая из-за сопряжения длина связи C¼C равна a, то длина двух связей в звене цепи сопряжения равна 2a, и расстояние между атомами N равно 2×(4+k) a.
Учтём дополнительную протяжённость электронного облака за пределы системы сопряжения, добавляя к ней ещё одну длину связи. В таком случае длина ящика L, в котором делокализован электрон, равна L= 2(4+k) a + a = (9+2k) a.
Подытожим только что полученные расчётные формулы:
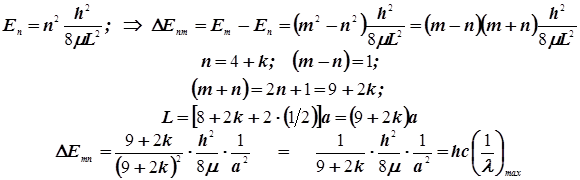
|
Необходимые постоянные в СГС:
m=9.1´10 -28 г (масса электрона),
c=3´1010 см/c (скорость света),
h = 6.62´10-27 э×c (константа Планка).
О размерности энергии 1 эрг=1э=1дн×см=1г×см×с2×см=1г×см2×с2.
Окончательно подставляем в формулу и получаем
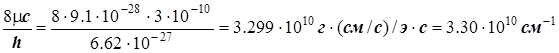
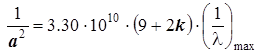
Можно вычислить усреднённую длину связи.
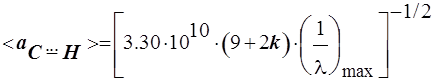
Вначале удобно вычислить величины 1/a2, затем их арифметически усреднить 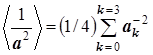 , и из усреднённого квадрата длины в завершение извлечь квадратный корень. Результат расчёта представлен в таблице в нижней клетке последнего столбца
, и из усреднённого квадрата длины в завершение извлечь квадратный корень. Результат расчёта представлен в таблице в нижней клетке последнего столбца
Это величина равна
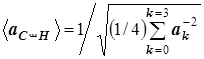 ,
,
Её-то и отождествим с искомым значением усреднённой длины связи СС.
Сравним результат с табличными данными.
У одинарная связи C-C в молекуле этана длина 1.53 А0.
У двойной связи C=C в молекуле этена длина 1.33 А0.
Длина выровненной связи C¼C в молекуле бензола 1.39 А0.
Простое арифметическое усреднение даёт a=1.43 А0
Расчёт из электронных спектров дал <a>=1.39 А0
в бензоле a=1.39 А0
Согласие удивительное !!! Особенно с бензолом !!!
Конечно же, нами был использован ряд приёмов подгонки .
В данной задаче продемонстрирован довольно типичный набор приёмов, которыми пользуются химики в отсутствие достаточно строгих способов расчёта молекулярных характеристик.
ДОМАШНЕЕ ЗАДАНИЕ по разделу:
Даниэльс-Олберти, стр. Раздел 15.14, задача-пример 15.6,
Задачи 15.64, 15.65
Информация о химии
Наночастицы позволят разобраться с термитами
Исследователи из Австралии обнаружили, что мезопористые наночастицы оксида кремния [mesoporous silica nanoparticles (MSN)] могут служить хранилищем и способом контролируемой доставки биоцидов. Такой способ доставки биологически ак ...
Ньюлендс (Newlands), Джон Александр Рейна
Английский химик Джон Александр Рейна Ньюлендс родился в Лондоне 26 ноября 1837 г. Отец, шотландский священник Уильям Ньюлендс, не хотевший, чтобы сын пошёл по его стопам, подготовил его к поступлению в в химический колледж. Мать, ...
Оседлав плазмонную волну
Исследователи из Калифорнийского Технологического Института продемонстрировали, как при возбуждении наночастицы лазерным излучением электрическое поле, окружающее эту частицу, изменяется как в пространстве, так и во времени. Появ ...