Производство этиленгликоля
Рефераты по химии / Получение хлористого винила / Производство этиленгликоляСтраница 1
Этиленгликоль СН2ОН—СН2ОН—бесцветная густая жидкость сладкого вкуса, температура кипения 197,2°С, температура плавления—13,2°С, удельный вес 1,114. Это простейший двуатомный спирт, хорошо растворимый в воде; водные растворы его замерзают при низкой температуре и применяются в качестве антифриза. Этиленгликоль употребляется как заменитель глицерина, например, в производстве ВВ, для синтеза некоторых органических веществ и в качестве добавок к веществам, устраняющим быстрое высыхание.
В процессе получения этиленгликоля образуются диэтиленгликоль и триэтиленгликоль. Эти вещества часто являются основными продуктами, выпускаемыми производством, при этом технологическая схема и режим работы его несколько меняются.
По описываемой схеме (Схема 6) этиленгликоль получается методом прямой гидратации окиси этилена без катализатора при давлении 10 атм. и температуре 165°С.
Основная реакция процесса:
СН2-СН2+Н20 → СН2ОН-СН2ОН.
v
О
Побочные реакции—образование дитриэтиленгликолей и полигли-колей.
СН2ОН-СН2ОН+СН2—СН2 → СН2ОН-СН2 - 0—СН2-СН2ОН
V
О
СН2ОН-СН2-О-СН2—СН2ОН+СН2-СН2 →
V
О
→ СН2ОН-СН2—О-СН2-СН2-О-СН2—СН2-ОН.
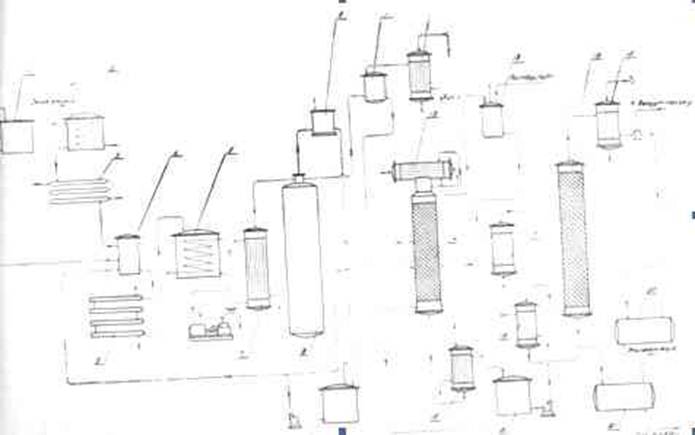
В качестве сырья применяют 98,5 %-ную окись этилена и паровой конденсат. Конденсат из сборника 1 и окись этилена из сборника 2, охлажденная в холодильнике 3 до 5—6°С, подаются в смеситель 4, куда поступает также обратный конденсат с температурой 30°С. Из него шихта, содержащая 10—15% окиси этилена и 88—90% воды по объему, направляется в трубчатый смеситель 6 и собирается в сборнике шихты 5, где поддерживается температура 5—6°С. Паровым насосом с давлением 10 атм. через подогреватель шихты 7 с температурой 130°С шихта подается в гидрататор 8, в котором протекает реакция получения этиленгликоля. Из гидрататора 8 реакционная масса дросселируется до 0,3 атм. в газосепаратор 11, откуда газовая фаза поступает в конденсатор 12, затем конденсат идет в напорный бак 1. Жидкая фаза из газосепаратора переходит в ректификационную колонну 14. Отгоняющиеся пары конденсируются в дефлегматоре 13 и поступают в сборник конденсата 18. Сюда же идет раствор щелочи для нейтрализации побочных продуктов реакции кислого характера. Конденсат из сборника 18 охлаждается в холодильнике 17 и направляется в смеситель 4. Из куба колонны вытекает 70%-ный этиленгликоль, который собирается в сборник 16. Центробежным насосом этиленгликоль подается через выносной кипятильник 15 во вторую ректификационную колонну 19 для отделения полигликолей. Пары этиленгликоля, выходя из колонны 19, конденсируются в конденсаторе 12. Конденсат, содержащий 70% этиленгликоля, собирается в сборник 20. Полигликоли, вытекающие из кубовой части колонны 19, собираются в сборнике 21 и направляются потребителю.
Основные параметры производства
Температура в гидрататоре 165°С
Давление в гидрататоре 10 атм.
Состав поступающей в гидрататор шихты:
окиси этилена 10—15% по объему
воды 80—90% по объему
Температура верха первой ректификационной колонны 100°С
Информация о химии
Tc — Технеций
ТЕХНЕЦИЙ (лат. Technetium), Тс, химический элемент VII группы периодической системы, атомный номер 43, атомная масса 98,9072. Свойства: радиоактивен, наиболее устойчивые изотопы 97Тс и 99Тс (период полураспада соответственно 2,6& ...
Химия полимеров
Химия полимеров — раздел химии, в котором изучаются химические свойства полимеров. Делится на разделы: физическая химия полимеров, структурная и т. д. Синоним — химия высокомолекулярных соединений — раздел орган ...
Выводы
1. Проведён анализ психолого-педагогической, методической и химической литературы для определения современного состояния проблемы применения эксперимента в системе проблемного обучения. 2.&nb ...


