Общие сведения по давлению паров
Рефераты по химии / Понятие давления паров и теплоты / Общие сведения по давлению паров
Согласно правилу фаз, давление паров чистой жидкости является однозначной функцией температуры насыщения, поэтому почти все данные о давлении паров представляют в виде зависимости
![]() .(7.1)
.(7.1)
Давление насыщенного пара ![]() может быть связано с любым другим интенсивным свойством насыщенной жидкости (или пара), однако температура насыщения в этом случае наиболее удобна. Если паровая фаза находится в равновесии с жидкой фазой, то условие равенства химических потенциалов, температуры и давления обеих фаз приводит к уравнению Клаузиуса-Клапейрона:
может быть связано с любым другим интенсивным свойством насыщенной жидкости (или пара), однако температура насыщения в этом случае наиболее удобна. Если паровая фаза находится в равновесии с жидкой фазой, то условие равенства химических потенциалов, температуры и давления обеих фаз приводит к уравнению Клаузиуса-Клапейрона:
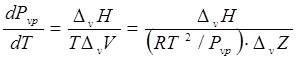 (7.2)
(7.2)
или
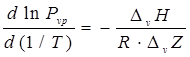 .(7.3)
.(7.3)
Большинство уравнений для расчета и корреляции давления паров получаются путем интегрирования уравнения (7.3). После интегрирования должна быть выбрана форма зависимости группы ![]() от температуры, а константа интегрирования определяется по одной точке “давление паров -температура”.
от температуры, а константа интегрирования определяется по одной точке “давление паров -температура”.
В общем случае зависимость ![]() от
от ![]() имеет S-образный вид. Для большинства веществ изменение наклона соответствует значению приведенной температуры
имеет S-образный вид. Для большинства веществ изменение наклона соответствует значению приведенной температуры ![]() =0,8-0,85. Для низкокипящих или неполярных соединений эта величина имеет более низкое значение (для метана точка перегиба
=0,8-0,85. Для низкокипящих или неполярных соединений эта величина имеет более низкое значение (для метана точка перегиба ![]() =0,7), для высококипящих, а также для полярных или ассоциированных жидкостей точка перегиба перемещается в область более высоких значений Tr (для этанола – 1,0).
=0,7), для высококипящих, а также для полярных или ассоциированных жидкостей точка перегиба перемещается в область более высоких значений Tr (для этанола – 1,0).
S-образный вид зависимости ![]() от
от ![]() обусловлен изменением отношения
обусловлен изменением отношения ![]() с температурой. Для нормальных жидкостей это отношение сравнительно нечувствительно к изменению температуры в диапазоне между нормальной температурой кипения вещества и его критической температурой. Объясняется это тем, что уменьшение теплоты парообразования компенсируется в некоторой степени уменьшением величины
с температурой. Для нормальных жидкостей это отношение сравнительно нечувствительно к изменению температуры в диапазоне между нормальной температурой кипения вещества и его критической температурой. Объясняется это тем, что уменьшение теплоты парообразования компенсируется в некоторой степени уменьшением величины ![]() . Ниже нормальной точки кипения (при
. Ниже нормальной точки кипения (при ![]() = 0,6-0,7) значение
= 0,6-0,7) значение ![]() очень близко к единице и изменение отношения
очень близко к единице и изменение отношения ![]() происходит исключительно вследствие изменения энтальпии.
происходит исключительно вследствие изменения энтальпии.
Информация о химии
Химия почв
Химия почв — это раздел почвоведения, изучающий химические основы почвообразования и плодородия почв. Основой для решения этих вопросов служит исследование состава, свойств почв и протекающих в почвах процессов на ионно-мол ...
Перрен (Perrin), Жан Батист
Французский физик Жан Батист Перрен родился в Лилле. Его вместе с двумя сестрами воспитывала мать, после того как их отец, офицер, умер от ран, полученных во время франко-прусской войны. Получив начальное образование в местных шко ...
Ле Шателье (Le Chatelier), Анри Луи
Французский физик и химик Анри Луи Ле Шателье родился в Париже. Его отец, горный инженер, принимавший участие в строительстве французских железных дорог, с раннего возраста прививал сыну любовь к наукам. Ле Шателье учился в коллеж ...


