Водородные связи с свойства органических соединений
Рефераты по химии / Водородная связь / Водородные связи с свойства органических соединенийСтраница 2
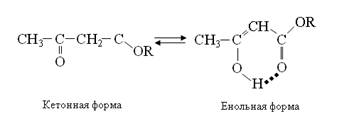
Образование энергетически менее выгодной енольной формы объясняется как формированием системы сопряженных связей С=С–С=О, что всегда является стабилизирующим фактором, так и тем обстоятельством, что между енольным гидроксилом и карбонильным кислородом образуется внутримолекулярная водородная связь, понижающая свободную энергию енольной формы как путем “закрепления” атома водорода у более электроотрицательного элемента, так и в результате удлинения цепи сопряжения (Н-связь включена в круговую цепь сопряжения). С учетом водородных связей не только объясняют реальность енольной структуры, но и количество этой формы в таутомерной системе. На состояние кето-енольного равновесия большое влияние оказывает природа растворителя. Максимальное количество енольной формы отмечается в нейтральных неполярных растворителях (углеводороды). В водных растворах количество енольной формы незначительно, так как вода конкурентно образует с карбонильным кислородом межмолекулярные водородные связи, разрушая стабилизирующие енольную форму внутримолекулярные водородные связи.
Карбоновые кислоты, как и спирты, могут участвовать в образовании Н-связей как в роли Н-доноров, так и Н-акцепторов. В первом случае кислотность снижается, во втором возрастает. Это ярко проявляется при ионизации двухосновных кислот: первая константа диссоциации (K1) аномально велика, а вторая (K2) аномально мала. Для объяснения наблюдаемых экспериментальных результатов кроме электронных эффектов большая роль придается вкладу Н-связей. В исходной структуре Н-связь сильно активирует карбоксильную группу, выступающую в роли Н-акцептора. В образовавшемся на первой стадии диссоциации моноанионе образуется прочная внутримолекулярная Н-связь, резко снижающая кислотность второго карбоксила:
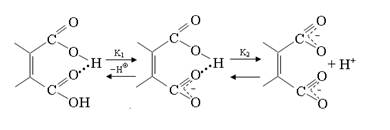
Для карбоновых кислот характерно образование Н-комплексов и ассоциатов псевдоциклической структуры:
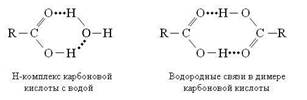
Межмолекулярные связи, возникающие между молекулами карбоновых кислот, настолько прочны, что даже в газообразном состоянии димерные структуры частично сохраняются. Кстати, образование димера карбоновой кислоты помогает дать ответ на давний вопрос, что в большей степени определяет прочность водородной связи – кислотность группы Х–Н или основность фрагмента В. Уксусная кислота (pKa= 4,7) по кислотности на несколько порядков уступая трихлоруксусной (pKa= 0,6), тем не менее образует более прочный димер. Основность протоноакцептора имеет приоритет перед кислотностью протонодонора.
Известно, что геминальные дигидроксипроизводные являются нестабильными соединениями – дегидратируясь легко превращаются в соответствующие альдегиды или кетоны. Хлоральгидрат является одним из немногих примеров, когда структура гем-диола является стабильной. И причину этого объясняют как сильным отрицательным индукционным эффектом (-I-эффект) трихлорметильной группы, так и наличием внутримолекулярных Н-связей:
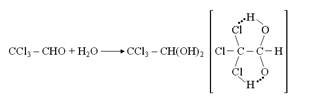
Не имея возможности остановиться на других примерах влияния водородной связи на свойства органических соединений, приведем таблицу сравнительных характеристик проявления меж- и внутримолекулярных Н-связей (табл. 1 (по [1])).
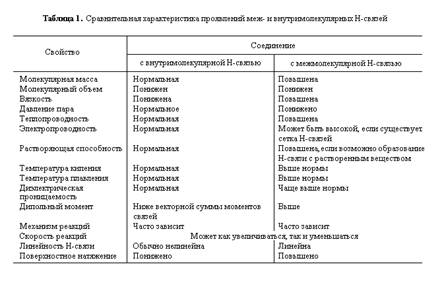
Образование внутри- и межмолекулярных водородных связей может существенно влиять на ход и скорость химических реакций. К сожалению, несмотря на значительное количество работ, посвященных этому вопросу, широких обобщений, которые имели бы предсказательную силу, не последовало. В самых общих чертах показано, что скорость реакций может уменьшаться или увеличиваться в зависимости от того, как при образовании Н-связи будет перераспределяться электронная плотность в реакционных центрах молекулы. Такие вопросы, как природа промежуточных продуктов или активированного комплекса, изменение термодинамических функций, влияние соседних групп, не получили должного развития. Более определенно дана оценка роли растворителя.
Информация о химии
Либавий (Libavius), Андреас
Немецкий химик и врач Андреас Либавий родился в Галле. Изучал философию, историю и медицину в Йенском университете. С 1581 г. был учитель в Ильменау, в 1586 г. – профессором в Кобурге. В 1586-1591 гг. – профессор истор ...
Ломоносов, Михаил Васильевич
Русский учёный Михаил Васильевич Ломоносов родился в селе Денисовка Архангельской губернии (ныне с. Ломоносово) в семье помора. В 1731 г. он поступает учиться в Славяно-греко-латинскую академию в Москве, выдав себя за дворянского ...
Химия древности
Химия, наука о составе веществ и их превращениях, начинается с открытия человеком способности огня изменять природные материалы. По-видимому, люди умели выплавлять медь и бронзу, обжигать глиняные изделия, получать стекло еще з ...


