Классификация ферментов
Рефераты по химии / Специфичность фермента амилазы / Классификация ферментовСтраница 2
Цитохром с Fe (II) + 4H+ + O2 > 4 Цитохром с Fe (III) + 2H2O
К моноксигеназам относят ферменты, катализирующие окисление органических соединений, приводящее к включению одного из атомов кислорода молекулы О2 в молекулы этих соединений, и восстановление второго атома кислорода до воды. Суммарное уравнение реакции можно записать в виде
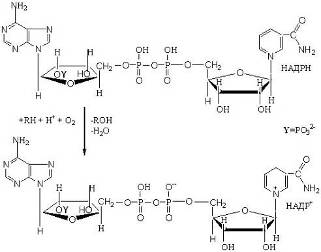
К монооксигеназам относится важная группа ферментов, известных под общим названием цитохромы Р450.
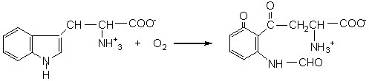
Диоксигеназы катализируют превращения, в ходе которых оба атома молекулы кислорода О2 включаются в состав окисляемого субстрата. Например, деструкция триптофана начинается с реакции образования формилкенуренина, в состав которого входят оба атома кислорода молекулы О2. Фермент, катализирующий эту реакцию, является гемопротеидом и называется триптофан 2,3-диоксигеназой.
Фермент, катализирующий диспропорционирование свободного радикала НO2, образующегося в некоторых реакциях с участием О2 и являющегося очень сильным окислителем, называют супероксидисмутазой. Он катализирует реакцию
HO2 + HO2 > H2O2 +O2
Фермент является металлопротеидом и в зависимости от источника содержит Cu2+, Zn2+, Mn2+, или Fe2+.
Трансферазы.
В этот класс входят ферменты, ускоряющие реакции переноса функциональных групп и молекулярных остатков от одного соединения к другому. В зависимости от характера переносимых группировок различают фосфотрансферазы, аминотрансферазы, гликозилтрансферазы, ацилтрансферазы, трансферазы, переносящие одноуглеродные остатки (метилтрансферазы, формилтрансферазы), и др.
Фосфотрансферазы. Сюда относят ферменты, ускоряющие реакцию переноса остатков фосфорной кислоты. К фосфотрансферазам относится, например, гексокиназа – фермент, ускоряющий перенос остатков фосфорной кислоты от молекулы АТФ к глюкозе (с этой реакции обычно начинается преобразование глюкозы):
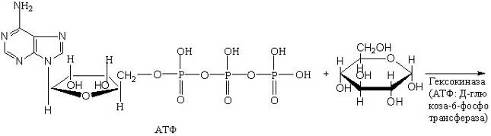
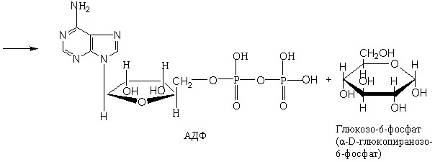
Аминотрансферазы. Эти ферменты ускоряют реакцию переаминирования аминокислот с кетокислотами и очень важны для обеспечения биосинтеза аминокислот. Они имеют следующее строение:
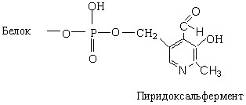
Пиридоксальфермент катализирует реакцию переаминирования. В результате серии реакций, включающих в себя непременное образование фермент-субстратных комплексов, аспаргиновая кислота переходит в щавелево-уксусную кислоту, а кетоглутаровая – в глутаминовую. Это выражается следующим суммарным уравнением:

Информация о химии
Мичерлих (Mitscherlich), Эйльгард
Немецкий химик Эйльгард Мичерлих родился в семье пастора небольшого селения Нёйенде на севере Германии. В 1811–1813 гг. он учился в Гейдельбергском и Парижском университетах, где изучал историю и культуру народов Востока. В ...
Нанокристаллы для белизны зубов
Исследователям из Германии удалось разработать новый класс стеклокерамических материалов с нанокристаллической структурой, который, вероятно, может идеально подходить для применения в стоматологии благодаря своей высокой прочности ...
Блэк (Black), Джозеф
Шотландский химик и физик Джозеф Блэк родился в Бордо (Франция); в 12-летнем возрасте переехал в Англию для получения образования. Он учился в Белфасте (Ирландия), а в 1746 г. поступил в университет в Глазго. Здесь он изучал медиц ...


