Прогнозирование энтропий органических соединений при повышенной температуре
Рефераты по химии / Энтропия органических веществ при нормальных и повышенных давлениях / Прогнозирование энтропий органических соединений при повышенной температуреСтраница 1
При прогнозировании энтропий органических веществ, находящихся при давлении 1 атм и температуре, отличающейся от 298 К, используются:
*
значение ![]() вещества, вычисленное любым из аддитивных методов или взятое из справочников;
вещества, вычисленное любым из аддитивных методов или взятое из справочников;
*
сведения о температурной зависимости теплоемкости вещества в виде аппроксимирующего уравнения или в табулированной форме;
* уравнение (2.4) для расчета температурной зависимости энтропии.
Процедура расчета иллюстрируется примером 2.4, при этом использованы справочные данные для теплоемкостей вещества, поскольку вопросы прогнозирования ![]() обсуждаются позже (разд. 3 данного пособия).
обсуждаются позже (разд. 3 данного пособия).
Пример:
Рассчитать ![]() окиси этилена при 400, 500 и 600 К. Энтропия
окиси этилена при 400, 500 и 600 К. Энтропия ![]() окиси этилена составляет 242,4 Дж/(моль×К) [1], значения теплоемкостей C0p,T при 400, 500 и 600 К заимствованы из [1] и приведены в табл. 2.6.
окиси этилена составляет 242,4 Дж/(моль×К) [1], значения теплоемкостей C0p,T при 400, 500 и 600 К заимствованы из [1] и приведены в табл. 2.6.
Решение:
С использованием уравнения (2.4) вычисляются энтропиии окиси этилена при интересующих температурах. При этом средние величины теплоемкостей окиси этилена считаются величинами постоянными для каждого из температурных диапазонов (от 300 до 400, от 400 до 500 и от 500 до 600 К) по условию создания таблиц, допускающему линейную интерполяцию соседних значений в них.
Результаты расчета приведены ниже и в табл. 2.6 сопоставлены с рекомендуемыми значениями [1].
![]() = 242,74+(48,53+62,55)/2·(ln400 –
= 242,74+(48,53+62,55)/2·(ln400 –
ln300) = 258,72 Дж/(моль×К);
![]() = 258,72+(62,55+75,44)/2·(ln500 –
= 258,72+(62,55+75,44)/2·(ln500 –
ln400) = 274,12 Дж/(моль×К);
![]() = 274,12 +(75,44+86,27)/2·(ln600 –
= 274,12 +(75,44+86,27)/2·(ln600 –
ln500) = 288,86 Дж/(моль×К).
Температурная зависимость ![]() иллюстрируется рис. 2.1.
иллюстрируется рис. 2.1.
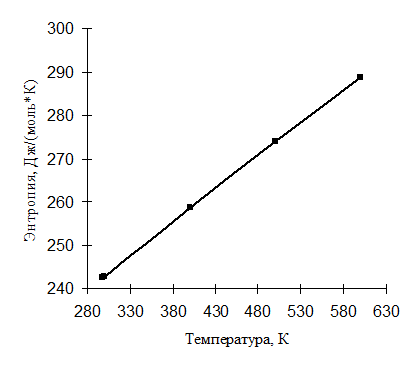
Рис. 2.1. Зависимость идеально-газовой энтропии окиси этилена от температуры
Таблица 2.6
|
Т, К |
|
|
|
Погрешность, % отн. |
|
298 |
242,42 |
48,28 | ||
|
300 |
242,76 |
48,53 |
242,74 |
0,00 |
|
400 |
258,65 |
62,55 |
258,72 |
0,03 |
|
500 |
274,01 |
75,44 |
274,12 |
0,04 |
|
600 |
288,78 |
86,27 |
288,86 |
0,03 |
Информация о химии
Химическая термодинамика
Тем временем химики обратились к центральному вопросу физической химии – о влиянии теплоты на химические реакции. К середине 19 в. физики Уильям Томсон (лорд Кельвин), Людвиг Больцман и Джеймс Максвелл выработали новые взгля ...
Mg — Магний
МАГНИЙ (лат. Magnesium), Mg (читается «магний»), химический элемент IIА группы третьего периода периодической системы Менделеева, атомный номер 12, атомная масса 24,305. Природный магний состоит из трех стабильных нукл ...
Крик (Crick), Фрэнсис Харри Комптон
Английский специалист в области молекулярной биологии Фрэнсис Харри Комптон Крик родился в Нортхемптоне и был старшим из двух сыновей Харри Комптона Крика, зажиточного обувного фабриканта, и Анны Элизабет (Вилкинс) Крик. Проведя с ...


