Исследование фазовых эффектов в бинарных азеотропных смесях
Рефераты по химии / Исследование фазовых эффектов в бинарных азеотропных смесяхСтраница 2
Состояние компонентов в фазах характеризуется при постоянном давлении и температуре их химическими потенциалами µ1 и µ2.
Будем различать фазовые эффекты общего типа, которые связаны с химическими потенциалами и фазовые эффекты частного типа, которые связаны с экстенсивными функциями. Обычно фазовые эффекты относят к той или иной фазе двухфазной системы.
На рисунке 1.1 изображены исследуемые диаграммы зеотропных смесей при T=соnst и Р=соnst.
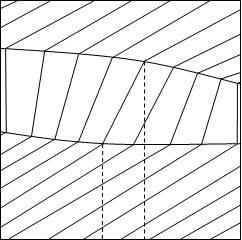
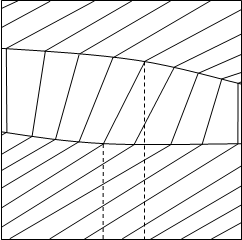 V S
V S
V2оп пар S2оп пар
V1оп S1оп
V2ож S2ож S1ож
V1ож
жидкость жидкость
х1 у1 х1,у1 х1 у1 х1,у1
a) б)
Рис.1.1. Диаграммы а) V - х, у, Т=const и б) S - х, у, Р=const
Вся диаграмма в этом случае имеет три области: область перегретого пара, область гетерогенности и область переохлажденной жидкости. Область пара от гетерогенной области отделена линией насыщенного пара, гетерогенная область отделена от области жидкости линией кипящей жидкости. В гетерогенной области проведены конноды жидкость-пар — отрезки, соединяющие состояние жидкости и пара. При Т=соnst равновесные составы имеют одинаковое давление и химические потенциалы компонентов, при Р=соnst равновесные составы имеют одинаковую температуру и одинаковые химические потенциалы компонентов. Конноды, как изотермо-изобары гетерогенной части, имеют после точек излома продолжение в областях пара и жидкости. Вдоль конноды жидкость-пар химические потенциалы не изменяются, а изменяется (скачком) объем и энтропия от Vж к Vп и от Sж к Sп. Вдоль же изотермо-изобар, так как давление и температура постоянны, справедливо уравнение Гиббса-Дюгема:
x1 dμ1ж+ x2 dμ2ж=0, y1 dμ1п+ y2 dμ2п=0. 1.3
т.е. химические потенциалы не постоянны.
1.2.Вид изотермо-изобар в бинарных смесях.
Образование раствора при постоянном давлении и температуре сопровождается повышением энтропии Sм и понижением Gм потенциала, при этом [2, 3]:
Hм=T Sм + Gм 1.4
Так как величина G при смешении меньше по сравнению с величиной, определяемой по аддитивности, а величина S больше по значению с величиной, определяемой по аддитивности, то различие между ними есть тепловыделение
|T Sм| < |Gм| 1.5
или теплопоглощение
|T Sм| > |Gм| 1.6
Учитывая, что H - G >0, изотермо-изобара всегда обращена выпуклостью вверх, т.е. в бинарной смеси
![]() 1.7 в то время как
1.7 в то время как ![]() 1.8
1.8
Это можно объяснить следующим образом. Так как температура кипения легколетучего компонента меньше температуры кипения тяжелолетучего компонента, то изотермо-изобара будет иметь на диаграмме S - x, y тангенс угла наклона положительный вдоль абсциссы x1. Эти свойства изотермо-изобары в бинарной смеси не зависят от того, рассматривается жидкая фаза или паровая. Однако эта кривизна изотермо-изобар очень мала, так как мала энтропия образования раствора. В качестве примера: энтропия образования 0,5 мольного раствора (х=0,5) идеальной смеси, т.е. максимальная энтропия образования равна:
Информация о химии
Кавендиш (Cavendish), Генри
Английский физик и химик Генри Кавендиш родился в Ницце; второй сын лорда Чарлза Кавендиша, герцога Девонширского. В 1749–1753 гг. обучался в Кембриджском университете, где заинтересовался естественными науками (надо отметит ...
Наночастицы позволят разобраться с термитами
Исследователи из Австралии обнаружили, что мезопористые наночастицы оксида кремния [mesoporous silica nanoparticles (MSN)] могут служить хранилищем и способом контролируемой доставки биоцидов. Такой способ доставки биологически ак ...
Крик (Crick), Фрэнсис Харри Комптон
Английский специалист в области молекулярной биологии Фрэнсис Харри Комптон Крик родился в Нортхемптоне и был старшим из двух сыновей Харри Комптона Крика, зажиточного обувного фабриканта, и Анны Элизабет (Вилкинс) Крик. Проведя с ...


