Первое начало термодинамики и его применение
Рефераты по химии / Первое начало термодинамики и его применениеСтраница 5
При термохимических расчетах реакций, протекающих в растворах, надо учитывать тепловой эффект процесса растворения химического соединения в данном растворителе.
Тепловой эффект образования химического соединения, диссоциирующего на ионы, определяется по теплотам образования ионов в растворе.
Теплота растворения зависит от концентрации химического соединения в растворе. Теплота, которая поглощается или выделяется при растворении одного моля вещества в таком количестве растворителя, чтобы образовался раствор с определенной моляльностыо т, называется интегральной теплотой растворения.
Теплота растворения твердого соединения с ионной кристаллической решеткой определяется в основном суммой двух величин: теплоты разрушения кристаллической решетки и теплоты сольватации ионов молекулами растворителя. В связи с тем, что на разрушение кристалла теплота затрачивается, а процесс сольватации сопровождается выделением теплоты, знак теплоты растворения может оказаться как положительным, так и отрицательным в зависимости от того, какое из двух слагаемых больше по абсолютной величине. Например, при растворении 1 моль СиС12*2Н20 в 8 моль воды поглощается 3,35 кдж теплоты; при растворении того же количества кристаллогидрата в 12 моль воды теплота растворения равна нулю; а при его растворении в очень большом количестве воды выделяется 17,67 кдж теплоты.
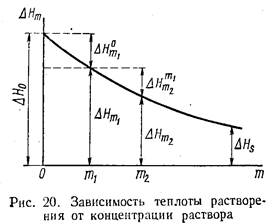
Зависимость интегральной теплоты растворения ΔНт от моляльности т раствора приведена на рис. 20. Значение ΔH равно первой интегральной теплоте растворения; оно равно тепловому эффекту при растворении одного моля вещества в бесконечно большом количестве растворителя; А Н0 определяется графической экстраполяцией ΔHт к т = 0. Отрезок ΔНя на рис. 20 соответствует последней или полной интегральной теплоте растворения; она равна теплоте растворения моля вещества в таком количестве растворителя, чтобы образовался насыщенный раствор.
Прибавление воды к раствору также сопровождается тепловым эффектом — теплотой разведения. Чем разбавленнее раствор, тем теплота разведения меньше. Пользуясь интегральными теплотами растворения, можно вычислить теплоты разведения. Различают две теплоты разведения — интегральную и промежуточную. Интегральной теплотой разведения ΔНт называют тепловой эффект, наблюдающийся при разбавлении раствора, содержащего один моль растворенного вещества, до бесконечного разведения, т. е. до т = 0.
Теплота растворения одного моля вещества в большом объеме* раствора определенной концентрации называется дифференциальной теплотой растворения.
При взаимодействии грамм-эквивалента сильной кислоты с сильным основанием в разбавленных водных растворах выделяется почти одинаковое количество тепла ДЯ = — 55,9 кдж/г-экв (при 25°С). Постоянство теплот нейтрализации связано с тем, что при взаимодействии сильных кислот и оснований, полностью диссоциированных в водных растворах, из ионов Н4" (точнее из ионов гидроксония Н30+) кислоты и ОН" основания образуются молекулы воды:
Н++ Сl + К++ОН=Сl +К+ + Н20(ж)
Нейтрализация слабых кислот сильными основаниями или сильных кислот слабыми основаниями сопровождается одновременной диссоциацией слабого электролита. При этом выделяется или поглощается теплота диссоциации ΔHДИСС, которая зависит от теплоты, поглощаемой при распаде молекулы на ионы, и теплоты гидратации ионов молекулами растворителя. Теплота диссоциации может быть как положительной, так и отрицательной. Таким образом, теплота нейтрализации слабых кислот и оснований складывается из двух величин: теплоты образования воды из ионов и теплоты диссоциации слабого электролита:
ΔH = — 55,9 + ΔHдисс, (II, 28)
где ΔH - теплота нейтрализации слабого электролита, кдж/моль\ АЯдисс — теплота диссоциации слабого электролита, кдж/моль.
Тепловые эффекты химических реакций с участием органических соединений удобно вычислять по теплотам сгорания, которые легко определяются из опыта. Теплотой сгорания называется тепловой эффект при постоянном давлении реакции окисления кислородом одного моля химического соединения с образованием продуктов сгорания. В качестве продуктов сгорания элементов С, Н, N, S и С1 принимают С02(г), Н20(ж), N2(r), SO2(r) и НС1(г).
Теплота сгорания, например, жидкого анилина представляет собой тепловой эффект реакции
C6H5NH2 (ж) + 7 02 (г) -> 6С02 (r)+3Н20 (ж) + N2
ΔHсг = — 3396 кдж/моль.
Вычисление тепловых эффектов реакций по теплотам сгорания производится на основании правила, являющегося следствием закона Гесса: тепловой эффект химической реакции равен разности между суммой теплот сгорания исходных веществ и суммой теплот сгорания продуктов реакции.
Информация о химии
Пуанкаре (Poincare), Жюль Анри
Французский математик и физик Жюль Анри Пуанкаре родился в г. Нанси. Учился в Политехнической (1873-1875), затем в Горной (1875-79) школах в Париже. С 1886 г. профессор Парижского университета. Был членом Бюро долгот (с 1893). Тру ...
Вант-Гофф (van't Hoff), Якоб Генрик
Нидерландский химик Якоб Генрик Вант-Гофф родился в Роттердаме, в семье врача Якоба Генрика Вант-Гоффа. По настоянию родителей Вант-Гофф начал изучать инженерное дело в Политехнической школе в Дельфте. В ней Вант-Гофф за два года ...
Физическая химия
Физи́ческая хи́мия — наука об общих законах физики и химии. Исследует химические явления с помощью теоретических и экспериментальных методов химии и физики. Начало физической химии было положено в середине XVIII в ...


