Производство серной кислоты
Рефераты по химии / Производство серной кислотыСтраница 5
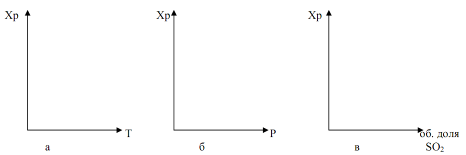
Тепловой эффект реакции зависит от температуры. Система «SO2 – О2 – SO3» характеризуется состоянием равновесия в ней и скоростью процесса окисления оксида серы (4), от которых зависит суммарный результат процесса.
Константа равновесия реакции окисления оксида серы (4) равна:
Кр = р8О3 / р8О2 *PO2,
где: рэО3, р8О2. рО2 – равновесные парциальные давления оксида серы (6), оксида серы (4), и кислорода соответственно.
Степень превращения оксида серы (4) в оксид серы (6) или степень контактирования, достигаемая на катализаторе, зависит от активности катализатора, температуры, давления, состава контактируемого газа и времени контактирования и описывается уравнением:
![]()
Где: рS03, где рS03 и рS02 – те же величины, что и в предыдущем уравнении.
Энергия активации реакции окисления оксида серы (4) кислородом в оксид серы (6) весьма велика. Поэтому в отсутствии катализатора реакция окисления даже при высокой температуре не идет. Применение катализатора позволяет снизить энергию активации реакции и увеличить скорость окисления.
В производстве серной кислоты в качестве катализатора применяют контактные массы на основе оксида ванадия (5) марок БАВ и СВД, названные так по начальным буквам элементов, входящих в их состав:
БАВ (барий, алюминий, ванадий) состава:
V205 (7 %) + K2S04 + ВаS04 + Al2(S04)3 + Si02 (кремнезем)

Предполагается, что процесс окисления оксида серы (4) на этих катализаторах идет через стадию диффузии реагентов к поверхности катализатора, на которой образован комплекс оксида ванадия (5) с активатором, сорбции реагентов на катализаторе с последующей десорбцией продукта реакции (оксида серы(6)):
V205 + S02 = V204 + S03, V204 + 0.502 = V205.
Температура зажигания контактных ванадиевых масс составляет 380–420оС и зависит от состава контактируемого газа, повышаясь с уменьшением содержания в нем кислорода. Обеспечение высокой температуры в начале процесса окисления требует больших затрат энергии на подогрев газа, поступающего на контактирование. Поэтому на практике температуру газа на входе в контактный аппарат, поступающего на первый слой катализатора, задают несколько выше температуры зажигания (4200С). В ходе реакции выделяется большое количество тепла и так как процесс в слое катализатора идет без отвода тепла, то температура газа повышается, после этого газ охлаждается в теплообменнике и направляется на второй слой катализатора, затем снова охлаждают и т.д. Таким образом, противоречие между кинетикой и термодинамикой процесса окисления оксида серы (4)
достаточно успешно снимается конструкцией и температурным режимом работы контактного аппарата на стадии, каждая из которых отвечает оптимальным условиям протекания процесса контактирования: температура 4000С, давление 0.1 Мпа, содержание оксида серы (4) в газе 0.07 об. долей, содержание кислорода в газе 0.22 об. долей.
Реакторы или контактные аппараты для каталитического окисления оксида серы по своей конструкции делятся на аппараты с неподвижным слоем катализатора (полочные, фильтрующие), в которых контактная масса расположена в 4–5 слоях и аппараты кипящего слоя. Отвод тепла после прохождения газом каждого слоя катализатора осуществляется путем введения в аппарат холодного газа или воздуха, или с помощью встроенных в аппарат или вынесенных отдельно теплообменников. Совокупность контактного аппарата, теплообменников и газопроводов представляет контактный узел.
Для увеличения конечной степени контактирования применяют метод двойного контактирования и ведут процесс окисления оксида серы в две стадии. На первой стадии контактирование ведут до степени превращения не превышающей 0.90–0.91 дол. единицы, после чего из контактированного газа выделяют оксид серы (6). Затем проводят вторую стадию контактирования до степени превращения оставшегося в газе оксида серы (4) 0.95 дол. единицы. Метод двойного контактирования позволяет повысить степень контактирования до 0.995 дол. ед. и на несколько порядков снизить выброс оксида серы (4) в атмосферу.
Абсорбция оксида серы.
Последней стадией в производстве серной кислоты контактным способом является абсорбция оксида серы (6) из контактированного газа и превращение его в серную кислоту или олеум.
Абсорбция оксида серы (4) представляет обратимую экзотермическую реакцию и описывается уравнением:
nSO3 + Н2О → H2SO4 + (n -1) SO3 + ДН
В зависимости от количественного соотношения оксида серы (6) и воды может быть получен продукт различной концентрации: при n >2 олеум, при n =1 моногидрат (100 % серная кислота), при n <1 водный раствор кислоты (разбавленная серная кислота).
Информация о химии
Кюри (Curie), Пьер
Французский физик Пьер Кюри родился в Париже. Он был младшим из двух сыновей врача Эжена Кюри и Софи-Клер (Депулли) Кюри. Отец решил дать своему независимому и рефлексирующему сыну домашнее образование. Мальчик оказался столь прил ...
Ибн Сина, Абу Али аль Хусейн ибн Абдаллах (Авиценна)
Персидский врач, учёный, философ и поэт Абу Али аль Хусейн ибн Абдаллах Ибн Сина (латинизированное имя – Авиценна) родился в с. Афшана, близ Бухары. Жил в Средней Азии и Иране, изучал в Бухаре математику, астрономию, философ ...
Дильс (Diels), Отто Пауль Герман
Немецкий химик Отто Пауль Герман Дильс родился в Гамбурге и был вторым из трех сыновей Германа Дильса, учителя и известного филолога, и Берты Дильс (в девичестве Дубель). Когда Отто исполнилось два года, семья переехала в Берлин, ...


